贝诺酯是解热镇痛抗炎药,其结构如图所示。下列有关说法正确的是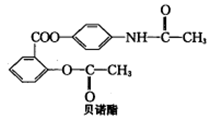
| A.分子式为C17H14O5N |
| B.在氢氧化钠水溶液中水解可以得到3种有机物钠盐 |
| C.1 mol贝诺酯与H2发生加成反应最多消耗8mol H2 |
| D.贝诺酯既属于酯类又属于蛋白质类 |
欲观察氢气燃烧的颜色,燃气导管口的材料最好是( )
| A.钠玻璃 | B.钾玻璃 | C.石英玻璃 | D.铜管 |
随着人们生活节奏的加快,方便的小包食品已被广泛接收。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
| A.无水硫酸铜、蔗糖 |
| B.硅胶、硫酸亚铁 |
| C.食盐、硫酸亚铁 |
| D.生石灰、食盐 |
白酒、食醋、蔗糖、淀粉均为家庭厨房中常用的物质,利用这些物质能完成的实验是( )
①检验自来水中是否含氯离子
②鉴别食盐和小苏打
③蛋壳能否溶于酸
④白酒中是否含甲醇
| A.①② | B.①④ | C.②③ | D.③④ |
下列说法正确的是( )
| A.淀粉和纤维素都是纯净物 |
| B.油脂是含热能最高的营养物质 |
| C.蔗糖能发生银镜反应 |
| D.人造丝、蚕丝的主要成分属于蛋白质 |
由锌、铁、铝、镁四种金属中的两种组成的混含物10 g,与足量的盐酸反应产生的氢气在标准状况下为11.2 L,则混合物中一定含有的金属是( )
| A.锌 | B.铁 | C.铝 | D.镁 |