炒河虾由青色变成红色,一同学认为这种红色物质可能是河虾体内某种物质在加热的时候发生颜色的改变。就这位同学的做法而言,这应该属于科学探究步骤中的
| A.实验 | B.观察 | C.假设 | D.分类 |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.60.0g二氧化硅晶体中,含有Si—O键的数目为NA |
| B.34g过氧化氢分子中极性共价键的数目为NA |
| C.标准状况下,22.4L甲烷和氨气的混合气体所含有的电子总数约为10NA |
| D.1molT2气体分子(超重氢分子)中所含的中子总数为2NA |
下列叙述中正确的是
| A.CO2分子内含有极性键,所以CO2分子是极性分子 |
| B.分子晶体、原子晶体中一定含有共价键,离子晶体中一定含有离子键 |
| C.气态氢化物的稳定性:NH3>PH3>AsH3 |
| D.某非金属元素从游离态变成化合态时,该元素一定被还原 |
科技日报2007年1月30日讯美、德两国科学家日前成功合成出具有独特化学性制质的氢铝化合物(AlH3)n,其结构类似于由B和H组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6的球棍模型如图。下列有关说法肯定不正确的是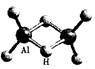
| A.Al2H6中H为+1价,Al为-3价 |
| B.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| C.Al2H6分子是非极性分子 |
| D.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
运用元素周期表分析下列推断,其中错误的是
| A.铍是一种轻金属,它的氧化物的水化物可能具有两性 |
| B.单质砹是一种有色固体,砹化氢很不稳定,砹化银是有色难溶于水且感光性很强的固体 |
| C.硫酸锶是难溶于水的白色固体 |
| D.硒化氢是无色、有毒,比硫化氢更稳定的气体 |
几种短周期元素的原子半径及主要化合价见下表
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+6,-2 |
+2 |
-2 |
下列叙述正确的是
| A.L、M的单质与稀盐酸反应的反应速率:M>L |
| B.R的氧化物对应的水化物可能具有两性 |
| C.T的气态氢化物分子间存在氢键 |
| D.L、Q形成的简单离子核外电子数相等 |