有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)/ mol·L-1为
| A.(y-2x)/a, | B.(y-x)/a, | C.(2y-2x)/a, | D.(2y-4x)/a。 |
一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:
2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
| 容器 编号 |
温度(℃) |
起始物质的量(mol) |
平衡物质的量(mol) |
|
| CH3OH(g) |
CH3OCH3(g) |
H2O(g) |
||
| I |
387 |
0.20 |
0.080 |
0.080 |
| Ⅱ |
387 |
0.40 |
||
| Ⅲ |
207 |
0.20 |
0.090 |
0.090 |
下列说法正确的是
A.该反应的正反应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
在25 ℃时,将0.2 mol CH3COONa晶体和0.1 mol HCl气体同时溶解于同一烧杯的水中,制得1 L溶液,若此溶液中c(CH3COO-)>c(Cl-),则下列判断不正确的是
| A.该溶液的pH小于7 |
| B.c(CH3COOH)+c(CH3COO-)=0.20 mol·L-1 |
| C.c(CH3COO-)+c(OH-)=0.10 mol·L-1 |
| D.c(CH3COOH)<c(CH3COO-) |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.28 g由C2H4和C3H6组成的混合物中含有氢原子的数目为4 NA |
| B.l mol Fe(NO3)3与足量HI溶液反应时转移的电子数为3NA |
| C.1 mol Na2O2固体中含离子总数为4NA |
| D.常温下,1 mol Fe与过量浓HNO3反应,转移电子的数目为3 NA |
向下图所示的装置中缓慢地通入气体X,若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞K,则品红溶液褪色。X和Y可能是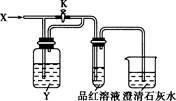
| A |
B |
C |
D |
|
| X |
SO2 |
C12 |
HCl |
NO2 |
| Y |
NaOH溶液 |
饱和NaHCO3溶液 |
饱和NaCl溶液 |
Na2SO3溶液 |
下列反应的离子方程式表示不正确的是
| A.漂白粉溶液在空气中长时间放置:ClO-+CO2+H2O = HClO+HCO |
| B.FeBr2溶液中通入少量Cl2:2Fe2++Cl2 =2Fe3++2Cl- |
| C.AgNO3溶液中加入过量稀氨水:Ag++2NH3·H2O = [Ag(NH3)2]++2H2O |
| D.SO2使氯水褪色:SO2+Cl2+2H2O =SO42-+2Cl-+4H+ |