近期陆续曝光了一些制药企业为了谋求暴利,用经生石灰处理过的皮革废料,熬制成工业明胶,制成药用胶囊。下列说法错误的是
| A.工业明胶是一种从动物的结缔或表皮组织中的胶原部分水解出来的蛋白质,其制备过程中因混有杂质,经常显现出鲜艳的颜色,因此可以将其作为食品添加剂中的着色剂使用 |
| B.此次曝光出的毒胶囊中有大家熟悉的阿莫西林胶囊。阿莫西林是一种最常用的青霉素类广谱抗生素,病人在使用青霉素前一定要进行皮试 |
| C.皮革在工业加工时,耍使用含铬的糕制剂,因此往往会造成铬含量的严重超标,重金属铬可使人体内的蛋白质变性 |
| D.生石灰与水的反应产物俗称熟石灰,其在工业生产上有很多用途,如治理酸性废水、制取漂白粉等 |
4、可以用分液漏斗进行分离的混合物是
| A.酒精和碘水 | B.苯和水 |
| C.乙酸和乙酸乙酯 | D.乙酸和水 |
3、下列物质中,不属于有机物的是
| A.尿素 | B.酒精 | C.苏打 | D.塑料 |
1、通常用于衡量一个国家石油化工发展水平的标志是
| A.石油的产量 | B.乙烯的产量 | C.天然气的产量 | D.硫酸的产量 |
3.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示,下列描述正确的是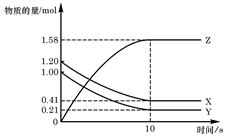
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s) |
| B.反应开始时10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始时10s,Y的转化率为79.0% |
D.反应的化学方程式为:X(g)+Y(g)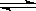 Z(g) Z(g) |
2.如图所示是298 K时N2与H2反应过程中 ,能量变化的曲线图.下列叙述正确的是
A.该反应的热化学方程式为:N2+3H2 2NH3 ΔH=-92 kJ/mol 2NH3 ΔH=-92 kJ/mol |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热改变 |
| D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1 |