标准状况下,1体积水中能溶解500体积的HCl气体。若向1 L水中通入标准状况下的448LHCl气体,假设气体完全溶解。
(1)若所得溶液密度为1.2 g/cm3,则溶液中含HCl物质的量浓度为 ;
(2)从该溶液中取出10mL浓盐酸溶解于水配制成500mL溶液,配制后的稀溶液中含HCl物质的量浓度为 。
(3)在用浓盐酸配制上述稀盐酸时,所用仪器中,使用前必须检查是否漏液的仪器有 ;配制过程中,造成浓度偏低的操作可能有_______________(选填下列操作的序号)。
| A.容量瓶蒸馏水洗后未加干燥 |
| B.量筒用蒸馏水洗后未干燥 |
| C.将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量中加水到刻度 |
| D.用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线 |
E、定容时,俯视液面加水至刻度线
下图中A~G均为中学化学中常见的物质,它们之间有如下转化关系。常温下,A为紫红色金属固体,B为常见的强酸,G为地壳中含量最多元素组成的气态单质;D、F都是大气污染物,主要来源于汽车尾气,D为无色气体,F为红棕色气体。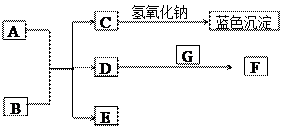
请回答以下问题:
①D的化学式是;C+NaOH生成的蓝色沉淀是(填化学式);
②构成G单质的元素在元素周期表中的位置为;
③写出B的稀溶液与A反应的化学方程式:。
下面是元素周期表的一部分,表中的每个字母表示一种短周期元素,请回答下列问题:
| A |
||||||||
| B |
C |
D |
E |
(1)D的最高价氧化物对应的水化物的化学式是__________。
(2)A、E两种元素中非金属较强的是___________(填元素符号)。
(3)B、C两元素的原子半径较小的是___________(填元素符号)。
(4)在盛有水的小烧杯中加入元素B的单质,发生反应的化学方程式为:
_________________________________________________________________________。
请根据题意选择下列物质:
| A.CH3COOH, | B.CH3CH2OH, | C.NaHCO3, | D.Na2O2,并用其字母代号填空: |
(l)能和碳酸钠反应生成二氧化碳的是;
(2)常用作为潜水艇呼吸面具中氧气来源的是;
(3)常用作溶剂,也可用作汽油替代燃料的是。
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成。乙醇和汽油经加工处理形成的车用燃料即乙醇汽油。
结合有关知识,回答下列问题:
(1)乙醇分子中的官能团是(填写名称)。
(2)试写出实验室用乙酸和乙醇在浓硫酸催化作用下共热反应生成乙酸乙酯的化学方程式 。
生活中常用药品很多,如:①碘酒、②麻黄碱、③青霉素、④阿司匹林、⑤葡萄糖注射液、⑥胃舒平(含氢氧化铝、淀粉等)。
(1)上述物质中属于抗生素的是_____(填写序号,下同),具有止咳平喘作用的天然药物是 。
胃舒平可防治胃酸分泌过多,其发挥功效时的离子方程式为 。
(2)低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是_________(填写字母,下同)。
| A.加成反应 | B.取代反应 | C.氧化反应 | D.聚合反应 |