据报道,一定条件下由二氧化碳和氢气合成乙醇已成为现实。
已知:①CH3CH2OH(l)+3 O2 (g)=2CO2(g)+3H2O(l) △H="-1366.8" kJ/mol
②2H2 (g)+O2 (g)=2H2O(l) △H="-571.6" kJ/mol
(1)写出由CO2和H2 反应合成CH3CH2OH (l)和H2O(l)的热化学方程式 。
(2)碱性乙醇燃料电池易储存,易推广,对环境污染小,具有非常广阔的发展前景。该燃料电池中,使用铂作电极,KOH溶液做电解质溶液。通入乙醇燃气的一极为 极,该极上的电极反应式为 。
(3)用乙醇燃料电池电解400 mL 饱和食盐水装置可简单表示如下图:
该装置中发生电解反应的方程式为 ;在铁棒附近观察到的现象是 ;当阴极产生448 mL气体(体积在标准状况下测得)时,停止电解,将电解后的溶液混合均匀,溶液的pH为 。(不考虑气体的溶解及溶液体积的变化)
X、Y、Z、U为原子序数依次增大的前四周期元素,X、Y、Z三种元素位于同一周期,其中基态Y原子的2p轨道处于半充满状态,Y和Z的单质可以通过分离液态空气的方法大量制得,且XZ2与Y2Z互为等电子体。含U的化合物的焰色为紫色。试回答下列问题:
(1)U单质的原子堆积方式为__________________,Y的价电子排布式为__________________。
(2)化合物甲由Z、U两元素组成,其晶胞如图所示。
①甲的化学式为____________。
②下列有关该晶体的说法中正确的是________(选填选项字母)。
A.每个晶胞中含有14个U+ 和13个Z2-
B.晶体中每个U+ 周围距离最近的U+ 有6个
C.该晶体属于离子晶体
③甲的密度为a g·cm-3,则晶胞的体积是_____________ m3(只要求列出计算式,阿伏加德罗常数的值用NA表示)。
Ⅰ.请按下列要求写出相应粒子的电子排布式,并回答有关问题:
(1)写出基态原子或离子的电子排布式:
Fe3+_________________;Cu _______________。
(2)比较 Fe2+与Fe3+的化学稳定性:Fe2+Fe3+;半径大小:Fe2+Fe3+(均填“>”或“<”)。
Ⅱ.(1)在第三周期中,第一电离能最小的元素是______,电负性最大的元素是_______(用元素符号表示)。
(2)第三周期原子中p轨道半充满的元素是_______(用元素符号表示)。
(3)第二周期原子中,未成对电子数等于其周期序数的原子有(用元素符号表示)。
Ⅲ.酞菁与酞菁铜染料分子结构如下图:酞菁分子中氮原子采用的杂化方式有:,并在下图相应位置上标出酞菁铜结构中铜原子周围的配位键: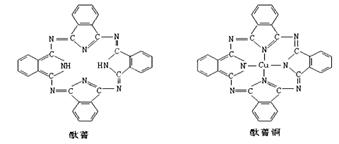
(1)甲醛易溶于水的原因是_______________________________________。
(2)沸点:甲醇_______甲醛(填“>”或“<”);原因:_________________________。
(3)为了减缓温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2 。若有2mol CH4生成,则有mol σ键和mol π键断裂。
(4)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为____________________________(填序号)。
实验室用下图所示的装置制取乙酸乙酯。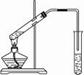
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液,其操作步骤为 ___________ ____________________________________,然后轻轻振荡试管使之混合均匀。
(2)装置中通蒸气的导管要插在饱和的Na2CO3溶液的液面上而不能插入溶液中,目的是防止溶液的倒吸。造成倒吸的原因是____________________________________________。
(3)浓硫酸的作用是:①__________________;②____________________。
(4)图中右边试管中试剂是_______________。
(5)分离得到乙酸乙酯的方法是__________,分离需要的玻璃仪器是____________________。
(6)若加的是C2H518OH写出制乙酸乙酯的方程式____________________________________。
(7)写出乙酸与碳酸氢钠反应方程式_____________________________________。
(1)某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,则烷烃结构式为______。混合气体中烷和烯的物质的量之比为_______________。
(2)某有机物A的相对分子质量为62。为进一步测定A的化学式,现取6.2 g A完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重5.4 g和8.8 g (假设每步反应均完全)。该有机物的实验式是_____,分子式是________。