短周期元素X、Y、Z在元素周期表中的位置如图所示。下列说法正确的是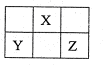
| A.原子半径的大小为:Z>Y>X |
| B.若X的一种单质为原子晶体,则含Y元素的盐溶液一定呈酸性 |
| C.若Y可作半导体材料,则X、Z的单质均为分子晶体 |
| D.若Y与Z的核电荷数之和为X的4倍,则X、Z各自形成的氢化物熔沸点:X<Z |
关于吸热反应的说法,正确的是( )
| A.凡需加热的反应一定是吸热反应 | B.只有分解反应才是吸热反应 |
| C.使用催化剂的反应是吸热反应 | D.酸碱中和反应的逆反应是吸热反应 |
下列各组离子能在指定溶液中,可能大量共存的是( )
①无色溶液中:K+、Na+、CO32—、SO42—
②pH=11的溶液中:Na+、Ba2+、AlO2—、ClO—
③水电离出的c(H+) =10—12mol·L—1的溶液中:Mg2+、NH4+、HCO3—、S2—
④加入Al放出H2的溶液中:Cu2+、NH4+、Cl—、NO3—
⑤无色溶液中:K+、Na+、 、
、 ⑥酸性溶液中:Fe2+、Al3+、NO3—、Cl—
⑥酸性溶液中:Fe2+、Al3+、NO3—、Cl—
| A.①②④ | B.①②④⑥ | C.①② | D.①②⑤ |
一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时。已知下表数据
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| Ksp(25 ℃) |
8.0×10-16 |
2.2×10-20 |
4.0×10-38 |
| 完全沉淀时的pH值 |
≥9.6 |
≥6.4 |
3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是( )
A.向该溶液中加少量铁粉不能观察到红色固体析出
B.该溶液中c(SO42-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
C.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
D.向该溶液中加入适量氯水,并调节pH值到3~4后过滤,得到纯净的CuSO4溶液
下列反应在任意温度下一定能自发进行的是( )
A.2NaCl+2H2O 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| B.NH3(g)+HCl(g)=NH4Cl(s) ΔH<0 |
| C.CaCO3(s)=CaO(s)+CO2(g) ΔH>0 |
| D.X2Y2(g)=X2(g)+Y2(g) ΔH<0 |
将pH=4的盐酸X L分别与下列三种溶液混合后,混合液均呈中性:
①1×10-4 mol/L的氨水Y L②c(OH-)=1×10-4mol/L的氨水Z L③c(OH-)=1×10-4 mol/L的Ba(OH)2溶液W L。其中X、Y、Z、W的关系正确的是( )
| A.Y>X=W>Z | B.X=Y>Z>W | C.X=Y>W>Z | D.Z>X=W>Y |