下列离子组在给定条件下能否大量共存的判断正确,所发生反应的离子方程式也正确的是
| 选项 |
条件 |
离子组 |
离子共存判断及反应的离子方程式 |
| A |
滴加氨水 |
Na+、Al3+、Cl-、NO3- |
不能共存,Al3++3OH-=Al(OH)3↓ |
| B |
pH=1的溶液 |
Fe2+、Al3+、SO42-、MnO4- |
不能共存, 5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O |
| C |
由水电离出的H+浓度为1×10-12mol/L |
NH4+、Na+、NO3-、Cl- |
一定共存,NH4++H2O NH3·H2O+H+ NH3·H2O+H+ |
| D |
通入少量SO2气体 |
K+、Na+、ClO-、SO42- |
不能共存, 2ClO-+SO2+H2O=2HClO+SO32- |
碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液.生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+ CH3OCOOCH3(g) 2 CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T),反应物配比(R=n(C2H5OCOOC2H5):n(CH3OCOOCH3))的关系如下图所示.三种反应物配比分别为1:1,2:1,3:1.下列说法不正确的是( )
2 CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T),反应物配比(R=n(C2H5OCOOC2H5):n(CH3OCOOCH3))的关系如下图所示.三种反应物配比分别为1:1,2:1,3:1.下列说法不正确的是( )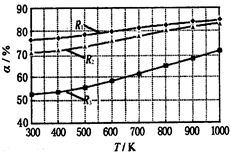
| A.该反应△H > 0 |
| B.R1对应的反应物配比为3:1 |
| C.650℃,反应物配比为1:1时,平衡常数K = 6 |
| D.该反应为取代反应 |
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是()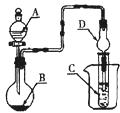
| A.若A为水,B为Al2S3固体,C中盛硫酸铜溶液,则C中有黑色沉淀生成 |
| B.若A为醋酸,B为贝壳,C中盛CaCl2溶液,则C中溶液变浑浊 |
| C.若A为浓氨水,B为碱石灰,C中盛氯化铝溶液,则C中溶液先出现白色浑浊后澄清 |
| D.若A为浓硫酸,B为铜,C中盛石蕊试液,则C中溶液褪色 |
普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述错误的是( )
| A.分子式为C23H36O7 |
| B.能使酸性KMnO4溶液褪色 |
| C.能发生加成,取代,水解,聚合,氧化反应 |
| D.1 mol 该物质最多可与1 mol NaOH 反应 |
下列解释事实的离子方程式正确的是( )
| A.向明矾溶液中加入氢氧化钡溶液至沉淀质量最大Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
| B.向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++HCO3-+OH- =CaCO3↓+H2O |
C.用惰性电极电解MgCl2溶液:2Cl-+2H2O 2OH- +Cl2↑+ H2↑ 2OH- +Cl2↑+ H2↑ |
| D.NaClO溶液中通入少量的SO2:ClO-+H2O+SO2=Cl-+SO42-+2H+ |
短周期元素R、T、Q、W在元素周期表中的相对位置如下图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是
| A.最简单气态氢化物的热稳定性:R>Q |
| B.最高价氧化物对应水化物的酸性:Q<W |
| C.原子半径:T>Q>R |
| D.含T的盐溶液一定显示酸性 |