某无色溶液X,由Na+、Ag+、Ba2+、Al3+、AlO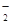 、MnO
、MnO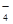 、CO
、CO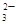 、SO
、SO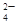 中的若干种离子组成,取溶液进行右图实验:
中的若干种离子组成,取溶液进行右图实验: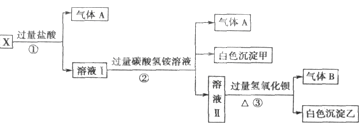
(1)白色沉淀甲是 。
(2)X溶液中一定存在的离子是 。
(3)白色沉淀乙中一定有: ,可能有 。
(4)若将过量的气体A与适量的气体B通入水中,写出反应的化学方程式 。
(15分)502胶,又名瞬干胶,有效成分是a—银基丙烯酸乙酯。因其固化速度快,使用方便,粘合力强,广泛应用于电器、医疗等行业。可由如下路线合成:
已知
②D是室内装潢时最常见的污染气体。
回答下列问题:
(1) B的结构简式是______,其名称(系统命名)是______。
(2) E的单体中含有的官能团是_______(写名称)。
(3) A与足量的NaOH水溶液共热时反应的化学方程式是__________________
(4) 写出C与D在碱性条件下反应生成聚合物E的化学方程式__________________
(5) X是C的同系物,且少一个碳原子,则X所有可能的结构简式有____________
(10分)下表是元索周期表前四周期的一部分,①〜⑤代表五种元素。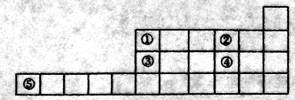
(1)⑤元素形成的一种离子在空气中很不稳定,写出此离子的核外电子排布式:______
(2) 标准状况下,①元素形成的气态氢化物与CO的密度相同,是一种高能燃料。1g该氢化物完全燃烧生成①的最高价氧化物(固态)和液态水放热72.35kJ。请写出该氢化物燃烧的热化学方程式:__________________。
(3) 染料工业排放的废水中含有大量有毒的NO2-,可以在碱性条件下加人③元素形成的单质除去。加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体。请写出相应的离子方程式:________________________。
(4) 分别写出含有④元素的某种18电子的微粒和含有②元素的某种10电子的离子间反应的离子方程式:__________________。
(1) 按系统命名法命名
①有机物CH3CH(C2H5)CH(CH3)2的名称是________________________。
②在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”。C7H16的同分异构体中具有“手性碳原子”的有三种,名称分别为________________________________________________ 。
(2) 写出下列各有机物的结构简式
① 2,3-二甲基-4-乙基已烷 _____________________________________
②支链只有一个乙基且式量最小的烷烃_____________________________
如图是由4个碳原子结合成的6种有机物(氢原子没有画出)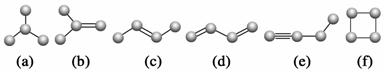
(1) 写出有机物(a)的系统命名法的名称______________。
(2) 有机物(a)有一种同分异构体,试写出其结构简式__ __。
(3) 上述有机物中与(c)互为同分异构体的是__ _ ___(填代号)。
(4) 任写一种与(e)互为同系物的有机物的结构简式____ _ ___。
(5) 上述有机物中不能与溴水反应使其褪色的有_____ ____(填代号)。
(6) (a)(b)(c)(d)(e)五种物质中,4个碳原子一定处于同一平面的有____________(填代号)。
有的油田开采的石油中溶有一种碳氢化合物——金刚烷,它的分子立体结构如图所示:
(1)由图可知其分子式为:____________。
(2)它是由_________ 个六元环构成的六体的笼状结构,其中有_________个,碳原子为三个环共有,连2个氢原子的碳原子数有个。