通过化学学习我们认识了许多的物质,请回答以下问题:
(1)氮气约占空气体积的 ;供给呼吸的气体是 .
(2)煤、石油和 是重要的化石燃料,大量使用化石燃料会使二氧化碳过多的排放,导致全球变暖.科学家采用高新技术,将二氧化碳和氢气在一定条件下组合,生成一种重要的化工原料乙烯(C2H4)和水,该反应的化学方程式为 .
(3)下列日常生活中的做法,符合“低碳生活”理念的是 (填字母,下同).
A.节约使用纸张 B.分类回收处理垃圾
C.减少使用塑料袋 D.减少使用一次性纸杯
(4)上海世博会在环保节能方面有一些新技术、新能源和新材料.下列表述不属于上述情况的是 .
A.太阳能的利用 B.地源热泵节能技术的使用
C.世博会开幕倒计时 D.园区内交通工具实现零排放
E、优化建筑设计,增强室内自然采光,减少照明用电.
利用下列仪器进行实验(所有装置的气密性都己检查完毕) 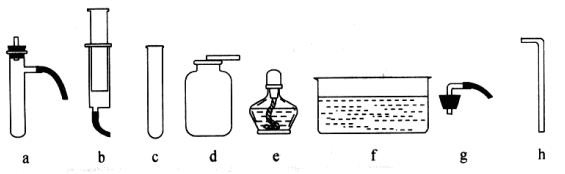
(1)图中编号为e的仪器的名称为。
(2)从上图中选出适当的仪器完成用“过氧化氢法”制取一瓶氧气的实验,并要求能够通过控制药品的添加量控制反应的快慢,你所选择的仪器有。用此装置除了可以制备氧气还可以制备二氧化碳气体,写出实验室制备二氧化碳的化学方程式。两种气体都可采用的收集方法是;检验二氧化碳已收集满的方法是。
(3)实验室制备氧气还有另一种方法,写出此反应的化学方程式。如果从上图仪器中选择并组装一套装置完成,完成这个实验还需添加的仪器是。
(6分)下列用字母表示的八种物质是由H、O、C、Na、Ca中的几种元素组成。
(1) A、B均由两种相同元素组成,其中A是人类生存所必需的物质之一,B在一定条件下能够分解得到A,则A的化学式为,写出B生成 A的化学方程式_________。
(2) D、E也是由两种相同元素组成,且在常温下均为气态氧化物,其中D可以作燃料,写出D转化为E的化学方程式_________。
(3) F、G均由3种元素组成,且属于同一类物质, G能转化为F,则F的化学式为,写出G转化为F的化学方程式_________。
(4) M在加热条件下可以生成A、E和另一种物质Q,写出这个反应的化学方程式_________。
物质都是由微小粒子构成的,化学反应的实质是粒子之间的重新组合。
(1)右图为甲、乙两种不同的气态物质在一定条件下反应生成丙物质的微观示意图,其中  和
和 分别表示氢原子和氮原子,则可知:
分别表示氢原子和氮原子,则可知: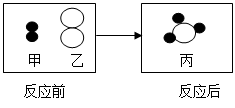
①在甲、乙、丙所表示的三种物质中属于单质的是。(填甲、乙、丙)
②构成丙物质的粒子是。(填“分子”、 “原子”或“离子”)
③此反应中甲、乙、丙三种物质的粒子个数比为。
(2)把一定质量的纯净物A和48g B在一定条件下按下图所示过程充分反应,当B消耗完时,可生成44 g D物质和18g E物质。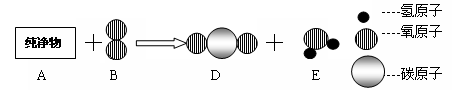
请回答下列问题:
①参加反应的A物质的质量是g。
②A分子中各元素的原子个数比是。(需表示出元素种类)
“ 溶液”在日常生产生活中应用广泛,因而我们要掌握一些有关“物质溶解”的知识。
(1)20℃时,17gKCl溶解在50g水中恰好达到饱和,则该温度下KCl的溶解度为g 。
(2)相同条件下,氢氧化铜难溶于水,高锰酸钾易溶于水,说明固体物质的溶解能力和溶质的性质有关;请你举例说明固体物质的溶解能力还与什么因素有关?(共1分)
| 影响固体物质的溶解能力 |
举例说明 |
(3)我们还发现,在用洗衣粉洗衣服时(在等量的水里放等量的洗衣粉),夏天洗衣粉很快溶解了,冬天反复搅拌后往往还会有许多洗衣粉颗粒悬浮水中,这说明洗衣粉的溶解度随着温度升高而______。当你用湿手取少量洗衣粉时,感觉手烫,你认为产生这种现象的原因是;若取用X固体代替洗衣粉与水混合,也得到与上述相似的现象,则加入的X固体可能是下列哪种物质。(填下列选项前的字母)
A.氧化钙B.硝酸铵 C.氢氧化钠D.氯化钠)
(4)下图为氯化铵和硫酸钠的溶解度曲线, 当把相同质量的氯化铵和硫酸钠的饱和溶液从50℃降到20℃时,析出晶体最多的是。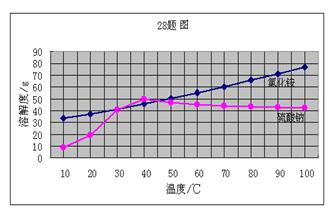
(5)在40℃时取两份100 g水分别往加入50克氯化铵和50克硫酸钠,充分搅拌后,升温到60℃,下列说法正确的是。
A.40℃时,两溶液均为饱和溶液
B.40℃时,两溶液质质量分数相等
C.50℃时.两溶液仍为饱和溶液
D.60℃时,硫酸钠溶液仍为饱和溶液,氯化铵溶液为不饱和溶液
E.60℃时,两溶液溶质质量分数相等
F.60℃时,两溶液中溶质质量分数不相等
3月11日,日本东北部地区发生9.0级地震,进而引发福岛第一核电站发生爆炸事故,“I-131” 一下子引起了人们极大的关注。
| 质子数 |
中子数 |
相对原子质量(近似取整) |
|
| I-127 |
m |
74 |
127 |
| I-131 |
53 |
n |
131 |
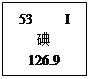
表1表 2
(1)碘是人体必需的微量元素之一,有“智力元素”之称。结合以上表1、表2的信息回答下列问题:
① I-127与I-131 属于同一种。(填元素、原子、分子)
② m与n 的数值依次是= 。(填写数值,共1分)
③ I-131一旦被人体吸入会引发甲状腺疾病,甚至可能引发甲状腺癌变。服用含碘元素的物质可封闭甲状腺,让放射性碘无法“入侵”。生活中常见的含碘元素的物质为:碘酒——含碘单质I2;碘片和藻类食物——含碘化钾KI;加碘盐——含碘酸钾KIO3 。下列对以上物质中碘元素的化合价计算正确的是:(填序号)
A. +1、-1、+5 B. 0、+1、+5 C. 0、-1、+5
(2)面对恐慌,掌握知识可以帮我们明辨是非。有人说“吃加碘盐可以防辐射”,我国规定在食盐中添加碘元素的标准为20-40mg/kg,若要达到防御碘-131辐射的作用,一次需补充碘元素100mg。按每人每天食用10g加碘盐,则我们每天最多能从碘盐中吸收 ______碘元素(填写质量,带单位)。
(3)核燃料所在反应堆芯因高温熔化是核电事故中最严重的事态。福岛第一核电站机组反应堆芯发生以上事故放出氢气,当接触外界的氧气后发生剧烈反应,导致连续爆炸。请写出有关氢气燃烧爆炸时的化学方程式为___________。
这次因冷却故障导致核反应堆发生爆炸,为中国核电站的快速扩张和核安全敲响了警钟,应该思考如何和平、安全利用原子能。下列说法中正确的是
A. 核能的利用证实原子的可分性 B. 核能的危害性太大,不应再推广使用
C. 开发核能可节约化石能源 D.核裂变是一种化学变化