用集气瓶可完成多种实验。请根据如下实验装置示意图,回答有关问题: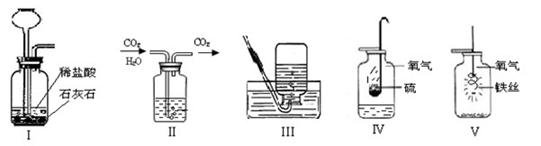
(1)装置Ⅰ完成的实验是 ________;为得到干燥的二氧化碳,装置Ⅱ的集气瓶中装入的试剂必须具有_____ 性。
(2)装置Ⅰ还可用于制取的气体的化学式是 ________,用装置Ⅲ收集该气体,其中水的作用是_________ ;装置Ⅳ的集气瓶中预先加入了少量水,猜测其作用可能是 ________;装置Ⅴ中的实验现象是_________。
(3)某同学做红磷在氧气中燃烧实验时,将点燃的红磷伸入盛有氧气的集气瓶中,红磷剧烈燃烧,过一会儿,燃烧匙内火焰熄灭。接着立即从集气瓶中取出燃烧匙,熄灭的红磷又复燃了。红磷复燃的原因是 ________ ;所以消防队员在火灾现场扑灭明火后,还要继续洒水的原因是 ________。
随着经济的发展,能源与环境成为人们日益关注的问题。。
(1) 海底埋藏着大量的“可燃冰”,其主要成分是甲烷水合物,甲烷的化学式为。
(2)氢气是最清洁的燃料,用化学方程式表示其原因。
(3)天然气、和煤被称为“化石燃料”。煤不充分燃烧时会产生大量的有毒气体,该气体是。燃煤发电时,将煤块粉碎成煤粉,其目的是。
(4)“绿色化学”的特点之一是“零排放”。一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物。其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是_______(填字母序号)。
| A.甲醇(CH4O) | B.甲酸(CH2O2) | C.乙醇(C2H6O) | D.乙酸(C2H4O2) |
水是重要的自然资源。
(1)如图A所示,试管2内得到的气体为,该实验可以证明水是由组成的;图B除去水中不溶性物质的方法是。 
A.水的电解 B.水的净化
(2)将源水处理成自来水的过程中需要加入适量的生石灰,目的是降低水的硬度,生石灰与水反应的化学方程式是。
(3)实验室的废液需经处理才能排放。为减弱含有硫酸的废液的酸性,不能选用的物质是(填字母序号)。
A.废铁钉 B.熟石灰 C.二氧化碳 D.碳酸钠
(4)下列做法中,有利于保护水资源的是(填字母序号)。
A.使用节水型马桶 B.合理使用农药和化肥
C.生活污水任意排放 D.工业废水处理达标后排放
生活中处处有化学,家庭厨房就是一个化学小世界。
(1)若锅里的油着火了,应立即盖上锅盖灭火,其原理是。
(2)水果和蔬菜富含的营养素是________(至少答两种)。
(3)食醋中含有醋酸(CH3COOH),醋酸由种元素组成,其中氢元素与氧元素的质量比为。
(4)为防止水龙头生锈,其表面镀有一层铬。铁生锈的条件是。
质量守恒定律应用的研究对化学科学发展具有重大作用。
(1)对质量守恒定律的微观解释是:在化学反应中,反应前后原子的、、都不改变。
(2)在一定条件下,将100 mL的CO2缓缓通过足量的淡黄色固体Na2O2,充分反应后,生成50mL纯净的气体X,X能使带火星的木条复燃,淡黄色固体部分变为白色固体Y。
友情提示:在同温同压下,气体的体积比等于分子个数比。
请回答:X气体是;该反应的化学方程式可表示为:a Na2O2+ b CO2 =" c" X + d Y (其中a、b、c、d为化学计量数),则b:c = ;已知a:b=1:1,则Y是。
(3)汽车安装安全气囊可以有效保护乘车人员,在车辆发生剧烈碰撞的瞬间,安全装置通电点火,使其中的粉末迅速分反应放出大量的氮气,形成气囊。该粉末由Fe2O3固体和化合物甲组成,加热13.0 g化合物甲,完全分解生成8.4 g氮气和单质乙。单质乙可在高温隔绝空气的条件下与Fe2O3发生置换反应生成Na2O。则化合物甲的化学式是。
有机高分子材料、金属材料和无机非金属材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少______污染。我们穿的衣服通常是由纤维织成的,区分棉纤维和羊毛纤维的方法是______。
(2)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于____(填“物理”或“化学”)变化。钢铁是制造轮船的主要金属材料,船身外通常装上比铁更活泼的金属块以防止腐蚀,该金属块可以选择______(选填“铜块”、“锌块”或“铅块”)。
(3)无机非金属材料中,用于电子工业的高纯碳酸钙和高纯氧化钙生产流程如下。
请回答:
①硝酸钙与碳酸铵在溶液中反应的化学方程式是Ca(NO3)2+(NH4)2CO3 = CaCO3↓+ 2NH4NO3,其基本反应类型为________。
②实验室常采用________操作进行沉淀分离。
③生产高纯碳酸钙时,选择“220℃恒温蒸发”,而不选择“高温”条件下完成此操作的原因是_______。