下列实验叙述正确的是( )
| A.新制氯水放置数天,溶液中的Cl2分子数目不变 |
| B.久置的氯水可使蓝色石蕊试纸先变红后褪色 |
| C.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| D.钠投入硫酸铜溶液中有红色粉末产生 |
下列说法正确的是()
| A.反应热就是反应中放出的能量 |
| B.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
| C.由C(石墨)→C(金刚石) ΔH=+1.9 kJ·mol-1可知,金刚石比石墨稳定 |
| D.在一定条件下,1 g碳燃烧所放出的热量为碳的热值 |
下列表示物质结构的化学用语或模型正确的是()
| A.7个中子的碳原子的核素符号:12C | B.HCl的电子式: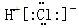 |
C.Cl-的结构式意图: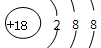 |
D.CH4分子的比例模型: |
X、Y、Z、W均为短周期元素,它们在周期表中的位置如下图所示。若X原子的最外层电子数比其次外层电子数多3个,下列说法错误的是( )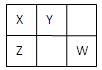
| A.原子半径:Z>X>Y |
| B.最高价氧化物对应水化物的酸性:Z>W |
| C.四种元素的氢化物中,Y的氢化物沸点最高 |
| D.阴离子的还原性:Z<W |
在强酸性溶液中,下列各组离子能大量共存的是( )
| A.Al3+、SO42-、NH4+ | B.Fe2+、NO3-、SO42- |
| C.Fe3+、OH-、SCN- | D.K+ 、Cl-、NO3- |
将铜片投入到稀硫酸中,铜片不溶,再加入下列试剂后,可使铜片溶解的是( )
| A.稀盐酸 | B.硫酸钠晶体 | C.硝酸钠晶体 | D.氯化铁晶体 |