将2.72g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得反应后放出标准状况下气体0.224 L.则下列判断中正确的是
| A.原混合物中n(Fe)∶n(Fe2O3)=3∶1 |
| B.反应后溶液中Fe2+和Fe3+的物质的量之比为3∶1 |
| C.实际参加反应HCl的物质的量为0.08mol |
| D.向溶液中滴入KSCN溶液,显红色 |
最近科学家确认世界上还存在的另一种“分子足球”N60,它与C60的结构相似。下列说法正确的是
| A.N60是一种新型化合物 | B.N60和N2是同素异形体 |
| C.N60和14N都是氮的同位素 | D.N60和N2是同分异构体 |
下列说法中错误的是
| A.测定中和热的实验中每次实验需要测定三次温度数据 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.凡经加热而发生的化学反应都是吸热反应 |
| D.反应物总能量和生成物总能量的相对大小决定了反应是放热还是吸热 |
北京时间2011年3月11日13时46分日本发生里氏9.0级大地震。地震导致的核泄露产生的放射性污染的主要成份是13153I和13755Cs,下列有关它们的说法正确的是
| A.铯137原子核内含有82个中子 |
| B.铯是金属性最强的元素,碘是非金属性最强的元素 |
| C.碘131的质子数是55,铯137的质量数是137 |
| D.碘元素在自然界有碘127和碘131两种稳定的同位素 |
某物质的分子式为CxHyOz,取该物质ag在足量的O2中充分燃烧后,将产物全部通入过量的Na2O2中,若Na2O2固体的质量增加了bg,并且a<b,则x、y、z必须满足的关系是
| A.x>z | B.x="y=z" | C.x="z" | D.x<z |
下列离子方程式正确的是
A.尼泊金酸与碳酸氢钠反应: |
| B.醋酸溶液与新制氢氧化铜反应:2 H++Cu(OH)2→Cu2++2H2O |
| C.苯酚钠溶液中通入少量二氧化碳:C6H5O—+ CO2 + H2O→C6H5OH+HCO3— |
| D.甲醛溶液与足量的银氨溶液共热 |
HCHO+2[Ag(NH3)2]++2OH-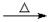
 CO32-+2NH4+ + 2Ag↓+ 2NH3+ H2O
CO32-+2NH4+ + 2Ag↓+ 2NH3+ H2O