Ⅰ.实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,下图中可选用的发生装置是 (填写字母)。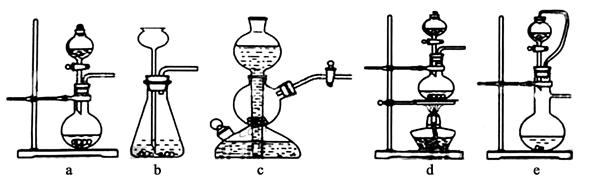
Ⅱ.A图表示某学生对SO2与漂粉精[80%Ca(ClO)2)]的反应进行实验探究的过程,观察到的现象有:
①.液面上方出现白雾;
②稍后,出现浑浊,溶液变为黄绿色;
③稍后,产生大量白色沉淀,黄绿色褪去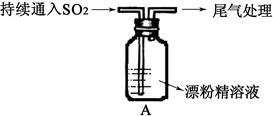
(1)向水中持续通入SO2,未观察到白雾。推测现象①中的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
由实验a、b不能判断白雾中含有HCl,理由是 。
(2)③中大量白色沉淀的成份是 。
(3)现象②中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和C1-发生反应产生了Cl2。通过进一步实验确认了这种可能性,其实验方案是 。
(4)用离子方程式解释现象③中黄绿色褪去的原因: 。
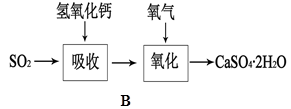
(5)B图表示石灰-石膏法吸收SO2的工艺流程,写出反应的化学方程式。
。
某兴趣小组的同学发现,将CuSO4溶液与Na2CO3溶液混合会产生蓝绿色沉淀。他们对沉淀的组成很感兴趣,决定采用实验的方法进行探究。
【提出猜想】
猜想1:所得沉淀为;
猜想2:所得沉淀为;
猜想3:所得沉淀为碱式碳酸铜[化学式可表示为mCu (OH)2·nCuCO3]。
查阅资料获知,无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【实验探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干。
步骤2:取一定量所得固体,用如下装置(夹持仪器未画出)进行定性实验。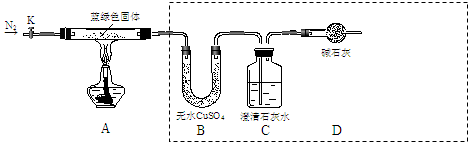
能证明猜想1成立的实验现象是。
【问题讨论】
(1)检查上述虚线框内装置气密性的实验操作是:关闭K,。
(2)若在上述装置B中盛放无水CaCl2,C中盛放Ba(OH)2溶液,还可测定所得沉淀的组成。
①C中盛放Ba(OH)2溶液,而不使用澄清石灰水的原因是。
②若所取蓝绿色固体质量为27.1 g,实验结束后,装置B的质量增加2.7 g,C中产生沉淀的质量为19.7 g。则该蓝绿色固体的化学式为。
氯气在工农业生产中应用非常广泛。请回答以下问题:
(1)下面是三位同学分别设计的实验室制取和收集氯气的装置,其中最好的是(填序号):
(2)某课外小组同学用如图所示装置通过电解食盐水并探究氯气相关性质,请回答: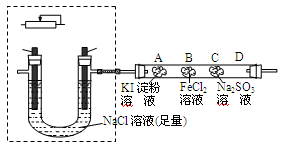
①现有电极:C和Fe供选择,请在虚框中补画导线、电源( ),串联变阻器以调节电流,同时标出电极材料;电解的离子反应方程式为。
),串联变阻器以调节电流,同时标出电极材料;电解的离子反应方程式为。
②通电一段时间后,玻璃管A、B、C三处是浸有不同溶液的棉花,其中A、B两处的颜色变化分别为、;C处发生的离子反应方程式为。
③为防止氯气逸出造成污染,应采取的措施是。
(3)当在阴极收集到气体448mL(标准状况)后停止实验,将U形管溶液倒于量筒中测得体积为400mL,则摇匀后理论上计算得溶液pH=。
利用某地的闪锌矿(主要成分为ZnS,其杂质主要为铁、铜元素等)冶炼纯锌的传统工艺如下: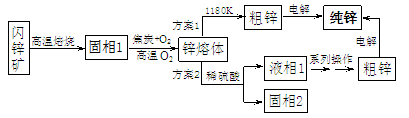
注:锌、铁、铜的沸点依次为1180K、2862K、1800K
(1)高温焙烧时,若氧气足量,则ZnS发生的化学反应方程式为。
(2)方案1由锌熔体获得粗锌的的操作为(填:“蒸馏”、“分馏”或“干馏”)。
(3)工业生产中方案2中固相2的成分为,液相1所含金属阳离子为:
(4)方案2中从液相1获取粗锌的过程中可用加入单质除掉其他杂质;对比两种方案,方案2的优点是。
(5)方案2的系列操作产生的废液可以制取绿矾。硫酸亚铁在不同温度下的溶解度和析出晶体的组成如下表所示:
| 温度/℃ |
0 |
10 |
30 |
50 |
56.7 |
60 |
70 |
80 |
90 |
| 溶解度 |
14.0 |
17.0 |
25.0 |
33.0 |
35.2 |
35.3 |
35.6 |
33.0 |
33.5 |
| 析出晶体 |
FeSO4·7H2O |
FeSO4·4H2O |
FeSO4·H2O |
从上表数据可以得出的结论是:①;②。
甲、乙组同学分别做了以下探究实验。
(1)甲组探究Cl2与Na2SO3溶液反应,实验装置如下。
①请指出该装置的不足之处、。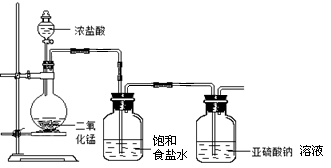
②Cl2与Na2SO3溶液反应的离子方程式为。
③设计实验,简述实验步骤,证明洗气瓶中的Na2SO3已被氧化。
乙组探究乙酸乙酯(沸点77.1℃)在不同温度、不同浓度NaOH溶液中的水解速率。
取四支大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积来确定水解反应的速率。
④请完成上表,其中V2 =,V4 =,V5 =。
⑤实验中,可用饱和食盐水替代蒸馏水,其优点是;但不能用饱和Na2CO3溶液替代蒸馏水,其原因是。
⑥实验中,试管Ⅳ比试管Ⅱ中的酯层减少更快,其原因有:温度高速率快,还可能有。
中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO4•7H2O)]中铁元素的含量。
①下列滴定装置中(夹持部分略去),最合理的是:(填字母序号)。
②实验前,首先要准确配制一定物质的量浓度的酸性KMnO4溶液250mL,配制时需要的仪器除托盘天平、玻璃棒、烧杯、胶头滴管、量筒外,还需要(填仪器名称)。
③该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10mol∙L-1FeSO4、0.02mol∙L-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。
 物理量 物理量实验序号 |
V[0.10mol∙L-1FeSO4] /mL |
KMnO4溶液褪色所需时间t/s |
||
| 1 |
a |
t1 |
||
| 2 |
a |
t2 |
(2)常温下,探究小组乙将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如右图所示。
①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)=。
②b点处溶液中c (Cl-) c (NH4+)(填“>”、“<”或“=”)。
③取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释:。
④d点所示溶液中离子浓度由大到小的排序是。