用系统命法写出下列物质名称或结构简式
(1)2,2,3-三甲基丁烷的结构简式是
(2)1,3-丁二烯的结构简式是
(3) 的系统命名是:
的系统命名是:
(4) 的系统命名是
的系统命名是
有机物A、B、C有如图所示转化关系,A的分子式为C3H4O2,A可与Br2的四氯化碳溶液发生加成反应,1 mol A能与1molNaHCO3溶液恰好完全反应。B所含元素种类与A相同,相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13%。试回答下列问题:
(1)A中所含官能团的名称为 。
(2)B的分子式为 ,B的同系物D的相对分子质量为60,则D可能的结构简式为 。
(3)A与B反应生成C的化学方程式为 ,该反应属于 反应。
(4)A、B的混合物共1mol,无论二者以何种比例混合,完全燃烧时下列量始终为定值的是 。
a.消耗氧气的量 b.生成水的量 c.生成二氧化碳的量
由硫可制得多硫化钠Na2Sx,x的值一般为2~6。当x=2时,多硫化钠称为过硫化钠。
Ⅰ.过硫化钠加入盐酸中有硫沉淀析出,写出该反应的化学方程式 ,该反应的还原产物是 。
Ⅱ.某些多硫化钠可用于制作蓄电池。下图是一种正在投入生产的大型蓄电系统的原理图。电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电的化学反应方程式为:

(1)电池中的左侧“电极”的电极名称是 (填“正极”或“负极”)。
(2)放电过程中钠离子从 (选“左到右”或“右到左”)通过离子交换膜。
(3)写出充电过程中阳极的电极反应式 。
在容积为2L的密闭容器中,进行反应:A(g)+2B(g) C(g)+D(g)
C(g)+D(g)
在不同温度下,D的物质的量n(D)和时间t的关系如图所示。试回答下列问题:
(1)800℃时,0—5min内,以B的浓度变化
表示的平均反应速率为 。
(2)能判断该反应达到化学平衡状态的依据
是 。
a.容器中压强不变
b.混合气体中c(A)不变
c.2v正(B)=v逆(D)
d.A、B、C、D四者共存
(3)该反应的正反应为 反应(填吸热或放热);判断的理由是 。
(4)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K(要求有计算过程)。
有①~⑧八种短周期元素,其原子序数依次增大,其中②、⑦、⑧三种元素在周期表中的相对位置如下,且元素②所处主族的位置为所有主族的正中间。
| ② |
|||
| ⑦ |
⑧ |
(1)元素②在周期表中的位置为 周期 族;②、⑦、⑧三种元素的原子半径由小到大的顺序是 (用元素符号表示)。②、⑦、⑧三种元素最高价氧化物对应水化物的酸性由强到弱的顺序是 (用化学式表示)。
(2)如图所示,甲、乙、丙、丁均为①~⑧中某些元素形成的单质或化合物,反应a为置换反应,反应b为化合反应(反应条件已略去),单质乙与单质丙所含元素位于同一主族,任写一个符合条件的反应a的化学方程式: 。
[化学——有机化学基础]
A、B、C、D四种芳香族化合物有的是药物、有的是香料。它们的结构简式如下所示:
A B C D
请回答下列问题:
(1)既能使FeCl3溶液显紫色又能和NaHCO3反应放出气体的有(用A、B、C、D填空)。
(2)1molA最多能与molH2发生加成反应。
(3)B分子中含有的官能团是______________(填写名称);B的同分异构体中,苯环上有两个邻位取代基,分别为“—OH”和含有“—COO—”结构的基团共有4种,其中两种(G和H)结构简式如下图所示,请补充另外两种。 、。
、。
(4)2006年齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭。D是“亮菌甲素”的结构简式,它配以辅料丙二醇溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性。 “亮菌甲素” 不能发生的反应类型是。
A.取代反应 B.消去反应 C.加成反应 D.氧化反应
(5)已知:①—COOH连接在苯环上,酸性显著增强。②醇和酸在催化剂作用下可直接反应生成酯,而酚不能。酚只能跟有机酸酐作用生成酯。例如: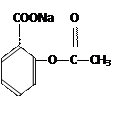

现以C为基本原料,请选择必要的其他反应物,用最佳途径合成
请写出其反应的化学方程式:
①;
②。