(1)同温同压下,同体积的NH3和H2S气体的质量比是___________;同质量的NH3和H2S气体的体积比是__________;同质量的NH3和H2S气体中所含氢原子个数比是___________;若两者所含氢原子个数相等,它们的物质的量比是________。
(2)Na2SO4••10H2O的摩尔质量是__________,483gNa2SO4••10H2O中所含Na2SO4••10H2O的物质的量是_______,所含Na+的物质的量是_________,所含H2O分子的数目是_______个。
在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
⑴该反应化学平衡常数的表达式:K=;
⑵该反应为(填“吸热”或“放热”)反应;
⑶下列说法中能说明该反应达平衡状态的是
A、容器中压强不变 B、混合气体中c(CO)不变
C、混合气体的密度不变 D、c(CO) = c(CO2)
E、化学平衡常数K不变 F、单位时间内生成CO的分子数与生成H2O的分子数相等
⑷某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为。
化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。下图为N2(g)和O2(g)生成NO(g)过程中的能量变化
(1)人们通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,则N≡N的键能为___________ kJ/mol,由上图写出N2(g)和O2(g)生成NO(g)的热化学反应方程式_______________________
(2)根据下列反应的热化学反应式,计算由C(石墨)和H2(g)反应生成1mol C2H2(g)的△H。
C(石墨) + O2(g) = CO2(g);△H1 =" -" 393.5 kJ/mol
2H2(g) + O2(g) = 2H2O(l);△H2 =" -" 571.6 kJ/mol
2C2H2(g) + 5 O2(g) = 4CO2(g) + 2H2O(l);△H3 =" -" 2599.2 kJ/mol,
则由C(石墨)和H2(g)反应生成1mol C2H2(g)的△H _______________________ kJ/mol。
已知稀的酸与稀的碱发生中和反应,生成1mol水所放出的热叫中和热,用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: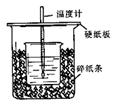
(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等、不相等”),所求中和热(填“相等、不相等”),
(3)已知滇池中学高二一班某同学的实验记录如下,
| 实验次数 |
酸的温度 |
碱的温度 |
反应最高温度 |
| 1 |
21.5℃ |
20.5℃ |
24.3℃ |
| 2 |
21.5℃ |
21.5℃ |
25.0℃ |
| 3 |
16.0℃ |
18.5℃ |
21.5℃ |
请根据有用数据计算中和热(酸碱的密度均视为1g/ml, C=4.17J/g.℃)
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”)。
部分中学化学常见元素原子结构及性质如下表所示:
| 序 号 |
元素 |
结构及性质 |
| ① |
A |
在地壳中的含量居于第三位,单质由电解法制取,其化学性质活泼,但在空气中能稳定存在;其离子半径在同周期中金属离子中最小。 |
| ② |
B |
B原子最外层电子数是内层电子数的1/5 |
| ③ |
C |
C单质分子中含化学键数最多,单质稳定,但其原子较活泼 |
| ④ |
D |
通常情况下,D没有正化合价,A、B、C、E都能与D化合 |
| ⑤ |
E |
E在周期表中可以排在IA族,也有人提出排在ⅦA族、ⅣA族 |
(1)上述元素中,其最高价氧化物对应的水化物呈两性的物质是_____________(填化学式),试用离子反应方程式表示其两性的原因___________________________________________;
_________________________________________________。
(2)B与C简单离子的半径大小为_________________(用离子符号表示)
(3)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,写出一定条件下X与B反应的方程式为,E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,请写出M的电子式,N的结构式 ___ __
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z单质的氧化性在同周期主族元素中最强。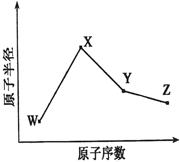
(1)X位于元素周期表中第周期第族;
(2)X的单质和Y的单质相比,熔点较高的是(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是(写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是。
(4)写出Z的单质与甲烷在光照的条件下发生第一步反应的方程式。