.下列叙述中正确的是()
| A.等质量的O2、O3中所含氧原子个数之比为2:3 |
| B.标准状况下,体积相等的CCl4和Cl2,前者含有的氯原子数是后者的两倍 |
| C.1molCO和CH4的混合气体所含的碳原子数和1molCO2所含的碳原子数相等 |
| D.10g NH3中含有原子数目约为4×6.02×1023 |
将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为()
A.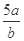 mol/L mol/L |
B. mol/L mol/L |
C. mol/L mol/L |
D. mol/L mol/L |
下列说法中正确的是 ( )
| A.1 mol/L的NaCl溶液是指由1 mol NaCl和1000mL水配制成的溶液 |
| B.从1 L 0.5 mol/L的NaCl溶液中取出100 mL,,剩余溶液物质的量浓度为0.45mol/L |
| C.0℃时,2 mol Cl2的体积可能为22.4 L |
| D.11.2L HCl气体通入水中,溶解后配成1L溶液,所得溶液物质的量浓度为0.5mol/L |
下列电离方程式书写正确的是()
| A.H2SO4=2H++SO42- | B.NaHCO3=Na++H++CO32- |
| C.KClO3=K++Cl-+3O2- | D.NaHSO4=Na++HSO4- |
下列各组物质分类正确的是 ( )
| 酸 |
碱 |
盐 |
氧化物 |
|
| A |
硫酸 |
纯碱 |
石灰石 |
水 |
| B |
盐酸 |
烧碱 |
纯碱 |
生石灰 |
| C |
碳酸 |
胆矾 |
熟石灰 |
干冰 |
| D |
干冰 |
苛性钾 |
食盐 |
石灰石 |