将空气除尘净化,除去二氧化碳和水蒸气后,在低温加压条件下使空气_______,然后控制温度分离液态空气,氮气沸点比氧气 ,先蒸发出来的是 ,余下的主要是 ,该过程为 (填“物理变化”或“化学变化”)。
下图是
三种物质的溶解度曲线,据图回答: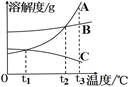
(1)℃时,
两种物质的溶解度相同;
(2)
℃时,将
三种物质的饱和溶液各
,分别蒸发
水,析出晶体最多的是。
钢铁在生产、生活中有着广泛的用途。请回答:
(1)炼铁厂常以焦炭、赤铁矿石(主要成分是
)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式:。
(2)每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。请你写出一种防止铁锅生锈的方法:。
2015年5月25日晚,河南鲁山县的一个老年康复中心发生火灾,造成38人死亡、多人受伤的严重后果。
(1)消防员在现场发现了下列残留物品:①涤纶面料窗帘、②纯棉床单、③大理石桌面等,其中属于有机合成材料的是(填序号),物品①和②为燃烧提供了(填燃烧的条件)。
(2)电器着火时常使用干粉灭火器灭火,干粉的主要成分是碳酸氢钠,受热后生成一种碳酸盐和两种氧化物,请写出该反应的化学方程式:。
今年3月22-28日是第28届"中国水周",其主题为"节约水资源,保障水安全。"
(1)下列关于水的说法中,不正确的有:(填序号)。
①水是由氢元素和氧元素组成的化合物
②清澈、透明的泉水是纯净物
③合理施用农药、化肥,以减少水体污染
④将活性炭放入硬水中可使其软化
⑤洗菜、洗衣后的水用来浇花、冲洗厕所
(2)自然界中的水一般要净化后才能使用。吸附、过滤、蒸馏等三种净化水的操作中,单一操作相对净化程度最高的是。
(3)下图表示自来水消毒过程中发生的一个反应的微观过程: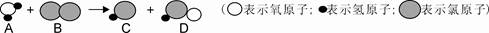
①写出上述物质中单质的化学式;
②物质
中氯元素的化合价为。
某饮用水标签上的部分文字如图,请回答:
(1)这里的钙、镁、钾、钠指的是(选填:原子、分子或元素)。
(2)钠原子的结构示意图是 ,其中x =。
,其中x =。