下列各组离子一定能大量共存的是
| A.在无色溶液中:NH4+、Fe2+、SO42-、CO32- |
| B.在含大量Ba2+的溶液中:Cu2+、Na+、Cl-、OH- |
| C.在强酸性溶液中:K+、Fe2+、Cl-、CH3COO- |
| D.在强碱溶液中:Na+、K+、Cl-、SO32- |
吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的“活性氧”,由此推断Na2SeO3的作用是
| A.做还原剂 | B.做氧化剂 |
| C.既做还原剂又做氧化剂 | D.既不做还原剂又不做氧化剂 |
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法正确的是: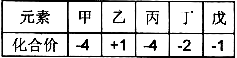
| A.乙的常见氧化物只有一种 |
| B.气态氢化物稳定性:丙>丁 |
| C.丙的氧化物能与戊的氢化物的水溶液反应 |
| D.原子半径大小:甲<丙 |
普罗帕酮为广谱高效抗心律失常药。下列说法正确的是: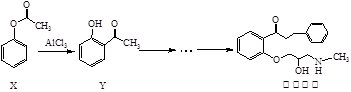
| A.可用溴水或FeCl3溶液鉴别X和Y |
| B.反应物X与中间体Y互为同系物 |
| C.普罗帕酮分子中有2个手性碳原子 |
| D.X、Y和普罗帕酮都能发生加成、水解、氧化、消去反应 |
下列图示与对应的叙述相符的是::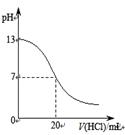
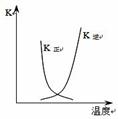
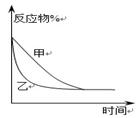
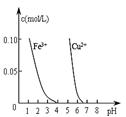
图a图b图c图d
| A.图a表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化 |
B.图b中曲线表示反应2A(g) + B(g) 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化 |
C.图c表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| D.据图d,若除去CuSO4溶液中的Fe3+ 可向溶液中加入适量CuO至pH在4左右 |
常温下,下列各组离子在溶液中一定能大量共存的是
| A.1.0mol/L的KNO3溶液:H+、Fe2+、Cl一、SO42一 |
| B.与铝反应产生大量氢气的溶液:Na+、K+、HCO3—、NO3一 |
C.pH=12的溶液: 、 、 、 、 、Br- 、Br- |
D.由水电离产生的 的溶液: 的溶液: 、 、 、 、 、 、 |