双氧水(H2O2)和水都是极弱的电解质,但H2O2比H2O更显酸性。
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:
(2)鉴于H2O2显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出H2O2与Ba(OH)2作用形成正盐的化学方程式: ,
(3)水电离生成H3O+和OH-叫做水的自偶电离。同水一样,H2O2也有极微弱的自偶电离,其自偶电离的方程式:
下列离子方程式书写正确的是
| A.铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B.AlCl3溶液中加入足量的氨水:Al3++ 3OH-=Al(OH)3↓ |
| C.饱和碳酸钠溶液中通入过量的CO2:CO32-+H2O+CO2 =2HCO3- |
| D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
某无色溶液能溶解Al(OH)3,则此溶液中一定能大量共存的离子组是
| A.Fe2+、Cl-、Na+、NO3- | B.K+、Na+、NO3-、HCO3- |
| C.Na+、Ba2+、Cl-、NO3- | D.Na+、K+、AlO2-、SO42- |
下列不能达到实验目的是
A B C D
| A.比较苏打和小苏打的热稳定性 | B.检查装置的气密性 |
| C.向容量瓶中转移溶液 | D.证明氨气极易溶于水 |
下列有关金属的说法正确的是
| A.金属单质在常温下都是固体 | B.金属原子只有还原性,金属阳离子只有氧化性 |
| C.含金属元素的离子都是阳离子 | D.金属阳离子被还原不一定生成金属单质 |
工业上用CO生产甲醇的反应为CO(g)+2H2(g)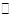 CH3OH(g)。图10表示反应中能量的变化;图11表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图。下列叙述错误的是
CH3OH(g)。图10表示反应中能量的变化;图11表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图。下列叙述错误的是

图10图11图12
| A.CO和H2合成CH3OH的反应:△H<0,△S>0 |
| B.保持温度不变,再充入1molCO和2molH2,反应达到新平衡时n(CH3OH)/n(CO)减小 |
| C.图10中曲线b可表示使用了催化剂的能量变化情况 |
| D.图12中曲线可表示在不同压强P1、P2(P1<P2)条件下甲醇百分含量随温度变化的情况 |