Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好PH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
【实验设计】控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
(1)请完成以下实验设计表(表中不要留空格)。
| 实验 编号 |
实验目的 |
T/K |
pH |
c/10-3mol·L-1 |
|
| H2O2 |
Fe2+ |
||||
| ① |
为以下实验作参考 |
298 |
3 |
6.0 |
0.30 |
| ② |
探究温度对降解反应速率的影响 |
|
|
|
|
| ③ |
|
298 |
10 |
6.0 |
0.30 |
【数据处理】实验测得p-CP的浓度随时间变化的关系如下图。
(2)请根据上图实验①曲线,计算降解反应在50~150s内的反应速率:
υ(p-CP)= mol·L-1·s-1
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:
。
(4)实验③得出的结论是:pH等于10时, 。
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法 。
下图所示装置进行有关实验,将A逐滴加入B中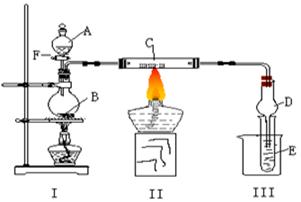
⑴若A是实验室的一种常用燃料,B是生石灰,实验中观察到C中黑色固体逐渐变红,当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁出现了光亮的银镜,则A是,C是,请写出反应管C中所发生的反应方程式:。试管E中所发生反应的离子方程式:。
⑵若I处酒精灯不加热, B、C仍是实验(1)中原物质,实验中也观察到C中黑色固体逐渐变红,同时可观察到E中溶液先形成沉淀,然后沉淀溶解,并有一种无色无味的气体逸出,当溶液恰好澄清时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁也出现了光亮的银镜,则A是,E中是与葡萄糖的混合液(写化学式)。请写出反应管C中所发生反应的方程式:。仪器D在此实验中的作用是。
⑶若B为浓硫酸,E为苯酚钠溶液,C仍旧不变,A是只含一个碳的一种有机物也能发生银镜反应,实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管中溶液变浑浊,则A可能是,然后往烧杯中加入沸水,可观察到试管中的现象是,此实验中浓硫酸的作用是。写出(1)中A和(3)中A二种物质在浓硫酸存在时所发生的反应方程式:,此反应中浓硫酸的作用是。
⑴如图所示,夹子开始时处于关闭状态,将滴管中液体A滴入试管②中,与气体B充分反应,打开夹子,可观察到试管①中96℃的水立即沸腾;则液体A和气体B的组合可能的是 。
A.氢氧化钠溶液;NO2气体 B.饱和食盐水;氯气
C.碳酸氢钠溶液;二氧化硫气体 D.氯化钙溶液;二氧化碳气体
⑵下列有关实验的叙述,不正确的是 。
A.白磷保存在水中,金属钠保存在煤油中,硝酸保存在棕色细口瓶中,且用磨口玻璃塞密封瓶口
B.用渗析法分离淀粉、KNO3 C.用氨水洗涤做过银镜反应的试管
D.用标准浓度的NaOH溶液测定未知浓度的盐酸,中和滴定前观察滴定管的液面高度为俯视,滴定终点时观察液面高度为仰视,测出的盐酸的浓度偏高
某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(忽略N2O4的存在,图中铁架台等夹持仪器均已略去):
Ⅰ.实验装置如下图1所示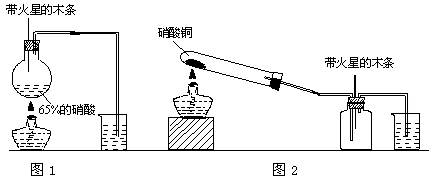
(1)浓硝酸受热分解的化学方程式是 。
(2)实验开始后木条上的火星逐渐熄灭,有的同学得出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确),理由是 。
Ⅱ.实验装置如上图2所示
(1)硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气,该反应的化学方程式是 。
(2)当集气瓶中充满红棕色气体时,木条复燃了,有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确”),理由是 。
Ⅲ.为了更直接说明“NO2能否支持木条的燃烧”这一问题,请你重新设计一个简单的实验方案,简述实验原理和主要操作。
某化学课外活动小组,从化学手册上查得硫酸铜在500 ℃以上按下式分解:CuSO4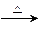 CuO+SO2↑+SO3↑+O2↑,便决定设计一验证性实验探索测定反应产生的SO2、SO3和O2的物质的量,并经计算以此确定该条件下CuSO4分解反应方程式中各物质的化学计量数。实验可能用到的仪器如下图所示:
CuO+SO2↑+SO3↑+O2↑,便决定设计一验证性实验探索测定反应产生的SO2、SO3和O2的物质的量,并经计算以此确定该条件下CuSO4分解反应方程式中各物质的化学计量数。实验可能用到的仪器如下图所示: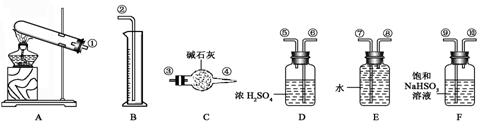
实验测得数据及有关结果如下:
①准确称取6.0 g无水CuSO4;②干燥管总质量在实验结束时增加了2.4 g;③测出量筒中水的体积后,折算成排水的气体,在标准状况下的体积为280 mL;④实验结束时,装置F中的溶液变为NaHSO4溶液(不含其他杂质,且O2在其中的损耗可忽略不计)。试回答下列问题:
(1)按装置从左至右的方向,各仪器连接顺序为(填代号)。
(2)装置F的作用是。
(3)装置D的作用是。
(4)确定装置E的进、出口的原则是:。
(5)首先应计算的是物质的体积;通过计算,推断出该条件下反应的化学方程式:
(6)该实验设计中,可能给测定带来误差最大的装置是___________________(填代号)。
某综合实践活动小组到自来水厂进行参观,了解到源水处理成自来水的工艺流程示意图如下:
⑴源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入CaO后生成Ca(OH)2,进而发生若干复分解反应,试写出其中的一个离子方程式。
⑵加入凝聚剂可以除去其中的悬浮固体颗粒,其过程是。(填写下列各项的序号)①只有物理过程,无化学过程②只有化学过程,无物理过程③既有化学过程又有物理过程;
FeSO4·7H2O是常用的凝聚剂,加入后,最终生成红褐色胶状沉淀,则这种红褐色胶状沉淀是。用化学反应方程式表示实验室制备该胶体的方法:
⑶通入二氧化碳的目的是和。
⑷气体A的作用是。
⑸下列物质中,可以作为气体A的代替品。(填写下列各项的序号)
①ClO2②浓氨水 ③SO2④浓硫酸