依据元素周期表及元素周期律,下列推断正确的是
| A.同一周期元素的原子,半径越小越容易失去电子 |
| B.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| C.若M+和R2-的核外电子层结构相同,则原子序数R>M |
| D.主族元素的最高正化合价等于该元素原子的最外层电子数 |
可逆反应:3A(g)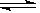 3B(?)+C(?)(正反应是吸热反应),随着温度升高,气体平均相对分子质量有减小趋势,则下列判断正确的是( )
3B(?)+C(?)(正反应是吸热反应),随着温度升高,气体平均相对分子质量有减小趋势,则下列判断正确的是( )
| A.B和C可能都是固体 | B.B和C一定都是气体 |
| C.若C为固体,则B一定是气体 | D.B和C可能都是气体 |
在10 ℃时,某化学反应速率为0.1 mol·L-1·s-1,若温度每升高10 ℃,反应速率增加到原来的2倍。为了把该反应速率提高到1.6 mol·L-1·s-1,则该反应需在什么温度下进行( )
| A.30 ℃ | B.40 ℃ | C.50 ℃ | D.60 ℃ |
如右图中的曲线是表示其他条件一定时,2NO+O2 2NO2(正反应是放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )
2NO2(正反应是放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )
| A.a | B.b | C.c | D.d |
已知:H2(g) + I2(g) 2HI(g)的平衡常数为K1;1/2 H2(g)+ 1/2 I2(g)
2HI(g)的平衡常数为K1;1/2 H2(g)+ 1/2 I2(g) HI(g)的平衡常数为K2,则K1、K2的关系为()。
HI(g)的平衡常数为K2,则K1、K2的关系为()。
| A.K1= 2K2 | B.K1= K22 | C.K1 = K2 | D.2K1= K2 |
已知:(1)H2(g)+1/2O2(g)  H2O(g) ΔH1=a kJ·mol-1
H2O(g) ΔH1=a kJ·mol-1
(2)2H2(g)+O2(g)  2H2O(g) ΔH2=b kJ·mol-1
2H2O(g) ΔH2=b kJ·mol-1
(3)H2(g)+1/2O2(g)  H2O(l) ΔH3=c kJ·mol-1
H2O(l) ΔH3=c kJ·mol-1
(4)2H2(g)+O2(g)  2H2O(l) ΔH4=d kJ·mol-1
2H2O(l) ΔH4=d kJ·mol-1
下列关系式中正确的是( )
| A.a<c | B.d>0 | C.2a=b<0 | D.2c=d>0 |