关于溶液的下列说法正确的是( )
| A.c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能大量存在 |
| B.水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在 |
| C.往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中增大 |
| D.等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3中c(CO32-)的大小关系为:②>④>③>① |
一定条件下反应mA(g)+nB(g) pC(G)+qD(g);ΔH<0。在一密闭容器中进行,测得平均反应速率v(C)=2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是()
pC(G)+qD(g);ΔH<0。在一密闭容器中进行,测得平均反应速率v(C)=2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是()
A. 2、6、3、5 B. 3、1、2、2 C. 3、1、2、1 D. 1、3、2、2
将10mL NO和NO2的混合气体通入装满水倒立在水槽中的量筒内,一段时间后,最后剩余4mL气体,原混合气体中含NO体积为()
| A.7mL | B.5mL | C.3mL | D.1mL |
漂白粉在溶液中存在下列平衡:ClO- + H2O 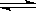 HClO + OH-,下列措施能提高漂白效果的是()
HClO + OH-,下列措施能提高漂白效果的是()
| A.加水稀释 | B.加入适量NaOH | C.通入少量SO2 | D.加入适量盐酸 |
下列电离方程式书写正确的是()
| A.NH3·H2O ="=" NH4++OH- | B.CuCl2 ="=" Cu2++Cl- |
| C.H2CO3 ="=" 2H++CO32- | D.Ba(OH)2 ="=" Ba2++2OH- |
在平衡体系2SO2(g)+O2(g) 2SO3(g)(正反应为放热反应),能使SO3的产量增加的措施是()
2SO3(g)(正反应为放热反应),能使SO3的产量增加的措施是()
| A.升高温度 | B.加入催化剂 | C.降低压强 | D.通入氧气 |