下列说法正确的是
| A.吸热反应在常温下一定不能发生 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.已知C(石墨,s)=C(金刚石,s),△H1>0,说明石墨比金刚石稳定 |
D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的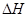 不同 不同 |
下列有关化学键与晶体结构说 法正确的是
法正确的是
| A.两种元素组成的分子中一定只有极性键 | B.离子化合物的熔点一定比共价化合物的高 |
C.非金属元素组成的化合物一定 是共价化合物 是共价化合物 |
D.含有阴离子的化合物一定含有阳离子 |
下列各组分子中都属于含极性键的非极性分子的是
| A.CO2、H2S | B.C2H4、CH4 | C.Cl2、C2H2 | D.NH3、HCl |
下列分子中所有原子都满足最外层为8电子结构的是
| A.BF3 | B.H2O | C.SiCl4 | D.PCl5 |
碘单质在水溶液中溶解度很小,但在CCl4中溶解度很大,这是因为
| A.CCl4与I2相对分子质量相差较小,而H2O与I2相对分子质量相差较大 |
B.CCl4与I2都是直线形分子,而H2O 不是直线形分子 不是直线形分子 |
| C.CCl4和I2都不含氢元素,而H2O中含有氢元素 |
| D.CCl4和I2都是非极性分子,而H2O是极性分子 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| D.氨气分子是极性分子而甲烷是非极性分子。 |