一定条件下,可逆反应C(s)+CO2(g)  2CO(g) ΔH>0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减小体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是 ( )
2CO(g) ΔH>0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减小体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是 ( )
| A.①②③④ | B.①③ | C.①② | D.①③④ |
下列行为中符合促进“低碳经济”发展宗旨的是:
①推广利用微生物发酵技术,将植物桔杆、动物粪便等制成沼气以替代液化石油气;
②利用硅材料制成光伏发电装置发电;③限制化学发展,关停化工企业,消除污染源
头;④大力发展潮汐能、风能、核能。
| A.①②④ | B.③④ | C.① | D.②④ |
某饱和一卤代烃的蒸汽对空气的相对密度为4.24,它与氢氧化钠的醇溶液共热,将产生的气体经过冷却、水洗、干燥后得到1.12升(标准状况)纯净气体,该气体通过足量溴水后,完全吸收,溴水质量增加2.1g。则此卤代烃的分子式为:
| A.C3H7Br | B.C3H6Br | C.C3H7I | D.C2H5I |
已知下列数据:
2Fe(s)+O2(g) =2FeO(s)△H=-544kJ·mol-1
4Al(s)+3O2(g) =2Al2O3(s)△H=-3350kJ·mol-1
则2Al(s) +3FeO(s) =Al2O3(s) + 3Fe(s)的△H是
| A.- 859 kJ·mol-1 | B.+859 kJ·mol-1 |
| C.-1403 kJ·mol-1 | D.-2491 kJ·mol-1 |
关于原电池的叙述正确的是
| A.原电池工作时,正极和负极上不一定都发生氧化还原反应 |
B.xLi+Li1-xNiO2 LiNiO2放电时此电池的负极材料是Li1-xNiO2 LiNiO2放电时此电池的负极材料是Li1-xNiO2 |
| C.在铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1120 mL(标准状况)气体析出 |
| D.在理论上可将该反应:CH4(g)+2O2(g)→CO2(g)+H2O(l) ΔH<0,设计成原电池 |
运动员服用兴奋剂是违背人文道德的。某种兴奋剂的结构简式如右图所示,有关该物质的说法错误的是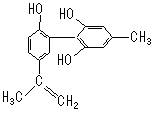
| A.滴入KMnO4(H+)溶液,观察紫色褪去 |
| B.遇FeCl3溶液不显颜色 |
| C.1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol |
| D.该分子中的所有碳原子可能共平面 |