工业生产水煤气的反应为:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.4 kJ/mol,下列判断正确的是( )
| A.反应物能量总和小于生成物能量总和 |
| B.CO(g)+H2(g)=C(s)+H2O(g) ΔH=+131.4 kJ/mol |
| C.水煤气反应中,生成1 mol H2(g)吸收131.4 kJ热量 |
| D.水煤气反应中生成1体积CO(g)吸收131.4 kJ热量 |
右图是元素周期表的一部分,下列说法中正确的是()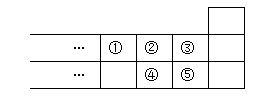
| A.元素①位于第二周期第ⅣA族 |
| B.气态氢化物的稳定性:④>② |
| C.最高价氧化物对应水化物酸性:⑤>④ |
| D.元素的最高正化合价:③=⑤ |
已知:①硫酸比次氯酸稳定;②高氯酸是比硫酸更强的酸;③S2﹣易被氯气氧化;④氯化氢比硫化氢稳定;⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应。上述叙述中可说明氯元素比硫元素非金属性强的是()
| A.①②③ | B.②③④ | C.③④⑤ | D.①③⑤ |
下列关于碱金属的叙述中不正确的是()
| A.碱金属元素的阳离子的氧化性随着原子序数的递增依次增强 |
| B.钾与氧气或水反应比钠的反应剧烈,铷、铯的反应更剧烈 |
| C.碱金属元素形成的单质的熔点随原子序数的递增而降低 |
| D.随着核电荷数的递增,他们最高价氧化物对应水化物的碱性逐渐增强 |
下列关于物质性质变化的比较,不正确的是()
| A.酸性强弱:HClO4>H2SO4>H3PO4>H2CO3 |
| B.原子半径大小:Na>S>O |
| C.稳定性:H2S>HCl>HBr>HI |
| D.金属性强弱:Na>Mg>Al |
对于反应A(g)+3B(g) 2C(g)+2D(g),下列四个数据是在不同条件下测出的该反应的速率,其中最快()
2C(g)+2D(g),下列四个数据是在不同条件下测出的该反应的速率,其中最快()
A. v(D) ="0." 4mol / (L·S) B. v(C) ="0." 5mol / (L·S)
C. v(B) ="0." 6mol / (L·S) D. v(A) ="0." 15mol / (L·S)