X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子。则这四种金属的活动性由强到弱的顺序为
| A.M>Z>X>Y | B.X>Y>Z>M | C.X>Z>Y>M | D.X>Z>M>Y |
有关元素的以下内容,随着原子序数的递增,不呈现周期性变化的是
| A.化合价 | B.原子半径 | C.最外层电子排布 | D.相对原子质量 |
元素周期表中某区域的一些元素多用于制造半导体材料,它们是
| A.左、下方区域的金属元素 |
| B.金属元素和非金属元素分界线附近的元素 |
| C.右、上方区域的非金属元素 |
| D.稀有气体元素 |
已知A、B为单质,C为化合物。
A+B C
C
 A+B
A+B
能实现上述转化关系的是()
①若C溶于水后得到强碱溶液,则A可能是Na
②若C的溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若C的溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.②④ C.①③ D.③④
以2010年诺贝尔化学奖获得者的名字命名的赫克反应、根岸反应和铃木反应已成为化学家们制造复杂化学分子的“精致工具”,在科研、医药和电子等领域已经广泛应用。下例生成物就是由铃木反应合成出来的一种联苯的衍生物:()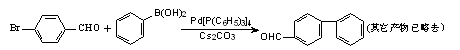
下列叙述正确的是()
| A.该反应为加成反应,且原子利用率达100% |
| B.该联苯的衍生物属于芳香烃 |
| C.该联苯的衍生物苯环上的一硝基取代产物有5种 |
| D.该联苯的衍生物不可使溴水褪色 |
某研究小组设计了如图所示的循环系统,来生产能 解决能源危机的某种物质,其中所需的电能由太阳能光电池提供。有关叙述正确的是()
解决能源危机的某种物质,其中所需的电能由太阳能光电池提供。有关叙述正确的是()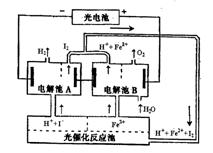
| A.设计该循环系统的目的是制取I2 |
| B.电解池A中离子反应方程式: H2+I2 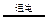 2H++2I- 2H++2I- |
| C.光催化反应池中离子反应方程式为: 2Fe2++I2 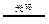 2Fe3++2I- 2Fe3++2I- |
| D.该系统中的Fe3+、H2O、I-都是循环使用的物质 |