某固体混合物可能由NaCI、K2SO4、CuCl2、CaCl2、K2CO3中的一种或几种混合而成,为鉴定其组成,依次进行如下实验:
混合物中加入足量水得到无色透明溶液;
(2)上述溶液中滴加BaCl2有白色沉淀产生;
(3)过滤,然后向上述白色沉淀中加盐酸时,沉淀全部溶解;
(4)往滤液中加AgNO3溶液时有白色沉淀产生且白色沉淀不溶于稀硝酸。
试判断:①肯定存在的物质有____________________________________;
②肯定不存在的物质有_______________________________;
③可能存在的物质有______________________________;
④写出第(4)步实验中发生反应的离子方程式:__________________________________。
某学生设计了如下图中的方法对A盐进行鉴定:
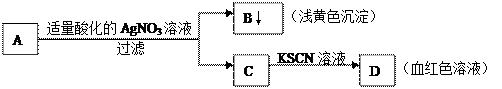 |
由此分析,下列结论中,正确的是
| A.A中一定有Fe3+ | B.C中一定有Fe3+ |
| C.B为AgI沉淀 | D.A一定为FeBr2溶液 |
下列各组离子在水溶液里能大量共存,但用盐酸酸化后,不能大量共存的是
| A.Na+、K+、Cl-、S2O32- | B.Al3+、K+、CO32-、SO42- |
| C.Al3+、Cl-、NO3-、NH4+ | D.Fe3+、K+、NO3-、SO42- |
下列实验装置设计正确,且能达到目的的是
极细的黄金粒子在水中可以形成玫瑰红色胶体金,为了能观察到胶体金颗粒的形态,德国化学家席格蒙迪研制出超显微镜,创立了现代胶体化学研究的基本方法,因而获得1925年的诺贝尔化学奖。用这种超显微镜能分辨的颗粒大小为
| A.10nm | B.200nm | C.1000nm | D.10000nm |
常温离子液体(又称常温熔融盐),是当前化学研究的热点和前沿。1914年报道的第一种离子液体硝酸乙基铵[(C2H5NH3)NO3]的熔点为12℃。已知C2H5NH2的化学性质与NH3相似,下列有关硝酸乙基铵的说法中,正确的是
| A.该离子液体可以作为电池的电解质 |
| B.硝酸乙基铵水溶液呈碱性 |
| C.(C2H5NH3)NO3能与NaOH反应产生NH3 |
| D.硝酸乙基铵水解的离子方程式可表示为:C2H5NH3++H2O=C2H5NH2+H3O+ |