I.(1)向Ba(OH)2溶液中加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式:________________________________。
(2)下列三种情况下,离子方程式与(1)相同的是_________________。
A.向NaHSO4溶液中逐滴加入Ba(0H)2溶液至显中性
B.向NaHSO4溶液中逐滴加入Ba(0H)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中逐滴加入Ba(0H)2溶液至过量
Ⅱ.实验室可以用氯酸钾和浓盐酸反应制取氯气,反应式如下:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)用双线桥法表示上述反应中电子转移的方向和数目。
(2)反应中发生氧化反应的物质是____________(填化学式),被还原的元素是____________________(填元素名称)。
(3)氧化剂与还原剂的物质的量之比为____________________。
(4)若反应中被氧化的盐酸为1mol,则生成的氯气体积为_______________(标准状况下)。
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐。现将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解。
(1)写出铜溶于上述混合溶液的离子方程式。
(2)若在如图Ⅰ所示的装置中发生(1)中的反应,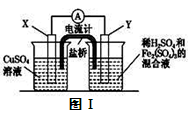
则X极是(“正极”或“负极”),电极反应式是
(3)铜完全溶解时,所得溶液中Fe3+、Cu2+、H+三种阳离子的浓度均为0.2 mol/L(假设溶液体积不变),若用电解方法回收铜,装置如图Ⅱ所示。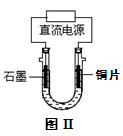
①电解开始阶段,阳极的电极反应式为,阴极的电极反应式为。
②判断溶液中的Cu2+已完全析出的现象是。当Cu2+恰好完全析出时,转移电子的物质的量。
I.在温度为T时,向2.0 L恒容密闭容器中充入1.0 mol A和1.0 mol B,发生反应A(g)+B(g)  C(g),一段时间后达到平衡。测定得部分数据见下表:
C(g),一段时间后达到平衡。测定得部分数据见下表:
| t/s |
0 |
5 |
15 |
25 |
35 |
| n(A)/mol |
1.0 |
0.85 |
0.81 |
0.80 |
0.80 |
回答下列问题:
(1)反应前5 s的平均反应速率v(A) =____________
(2)温度为T时,该反应的化学平衡常数=
(3)升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH(填 “>0” 或 “<0”)
(4)相同温度下,起始时向容器中充入0.2 mol A、0.2 mol B和1.0 mol C,反应达到平衡前,反应速率v正v逆(填“>” 或 “<”)
(5)下列措施能增大反应速率,且平衡往正反应方向移动是。
a.及时分离出A气体
b.适当升高温度
c.增大B的浓度
d.选择高效催化剂
II.NO、NO2是常见的氧化物。用H2或CO催化还原NO可达到消除污染的目的。
已知:2NO(g) = N2(g) + O2(g) △H = -180.5kJ·mol-1
2H2O(l) = 2H2(g) + O2(g) △H = +571.6kJ·mol-1
则用H2催化还原NO消除污染的热化学方程式是
(12分)已知:
(X为卤原子,M为烃基或含酯基的取代基等)
由有机物A合成G(香豆素)的步骤如下: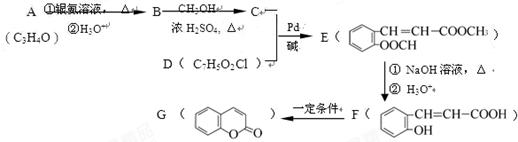
回答下列问题:
(1)写出A中所含官能团名称:,F→G 的反应类型是。
(2)写出B→C的化学方程式。(3)D的结构简式为。
(4)F有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式:。
Ⅰ.分子中除苯环外,无其它环状结构;
Ⅱ.苯环上有两个处于对位的取代基;
Ⅲ.能发生水解反应,不能与Na反应;
Ⅳ.能与新制Cu(OH)2按物质的量比1:2反应
(5)二氢香豆素(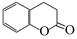 )常用作香豆素的替代品,鉴别二氢香豆素和它的一种同分异构体(
)常用作香豆素的替代品,鉴别二氢香豆素和它的一种同分异构体(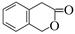 )需要用到的试剂有:NaOH溶液、。
)需要用到的试剂有:NaOH溶液、。
(6)已知: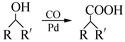 (R,R′为烃基),试写出以苯和丙烯(
(R,R′为烃基),试写出以苯和丙烯(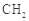 =CH—CH3)为原料,合成
=CH—CH3)为原料,合成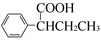 的路线流程图(无机试剂任选)。合成路线流程图示例如下:
的路线流程图(无机试剂任选)。合成路线流程图示例如下: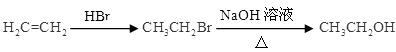
工业上以铬铁矿(主要成分FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O)的主要反应如下:
①4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
②2Na2CrO4+H 2SO4 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
(1)工业上反应①需不断搅拌,其目的是。
(2)下图是红矾钠(Na2Cr2O7·2H2O)和Na2SO4的溶解度曲线。
从Na2Cr2O7和Na2SO4的混合溶液中提取Na2Cr2O7晶体的操作:
先将混合溶液蒸发结晶,趁热过滤。趁热过滤的目的是;然后将滤液,从而析出红矾钠。
(3)Na2Cr2O7与KCl进行复分解反应可制取K2Cr2O7,现用重铬酸钾测定铁矿石中铁的含量,测定原理为:Fe2++Cr2O72-+H+ Fe3++ Cr3+ +7H2O (未配平)
Fe3++ Cr3+ +7H2O (未配平)
实验步骤如下:
步骤1:将m g铁矿石加浓盐酸加热溶解步骤2:加入SnCl2溶液将Fe3+还原
步骤3:将所得溶液冷却,加入HgCl2溶液,将过量的Sn2+氧化为Sn4+
步骤4:加入15 mL硫酸和磷酸的混合酸及5滴0.2%二苯胺磺酸钠指示剂
步骤5:立即用c mol·L-1重铬酸钾溶液滴定至溶液呈稳定紫色,即为终点,消耗重铬酸钾溶液V mL
①如省去步骤③,则所测定的铁的含量(填“偏高”、“偏低”或“无影响”)。
②步骤5使用的主要玻璃仪器有。
③则测定铁矿石中铁的含量的计算式为(用字母表示,不用化简)。
近年来雾霾天气在秋冬季节经常肆虐我国中东部地区。其中,汽车尾气和燃煤是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO (g)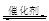 2CO2 (g) +N2 (g)
2CO2 (g) +N2 (g)
在某密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。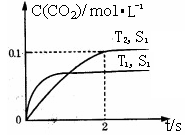
据此判断:
①该反应的平衡常数表达式为。
②该反应的ΔH0(选填“>”、“<”)。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在右图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g)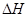 =-867kJ·mol-1
=-867kJ·mol-1
2NO2(g)  N2O4(g)
N2O4(g)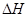 =-56.9kJ·mol-1
=-56.9kJ·mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。右图是通过光电转化原理以廉价原料制备新产品的示意图。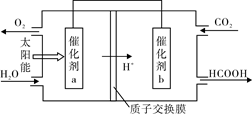
写出上述光电转化过程的化学反应方程式。催化剂a、b之间连接导线上电子流动方向是(填a→b或b→a) 。