氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据上图,完成下列填空:
(1)与电源负极相连的电极附近,溶液pH值(选填:不变、升高或下降),与电源正极相连的电极叫 极,检验该极上产物的方法是 。
(2)写出电解饱和食盐水的化学方程式 。
(3)如果粗盐中SO 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO ,该钡试剂可以是(选填A.B.c,多选扣分)
,该钡试剂可以是(选填A.B.c,多选扣分)
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(4)判断钡试剂已经过量的方法是 。
(5)为有效除去Ca2+、Mg2+、SO ,加入试剂的合理顺序为(选填a,b,c多选扣分)
,加入试剂的合理顺序为(选填a,b,c多选扣分)
A.先加NaOH溶液,后加Na2CO3溶液,再加钡试剂
B.先加NaOH溶液,后加钡试剂,再加Na2CO3溶液
C.先加钡试剂,后加NaOH溶液,再加Na2CO3溶液
(6)为检验精盐纯度,需配制150 mL0.2 mol/LNaCl(精盐)溶液,下图是该同学转移溶液的示意图,图中的错误是 。
CO、O2、CO2混合气体9mL电火花引爆后,恢复到原来状态时,气体体积减少1mL,通过NaOH溶液后,体积又减少5mL,则混合气体中CO、O2、CO2体积比可能为 _____ 。
现有m g某气体,它由四原子分子构成,它的摩尔质量为M g·mol-1。则:
(1)该气体的物质的量为________。
(2)该气体中所含的原子总数为________个。
(3)该气体在标准状况下的体积为________L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为________。
对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、加热分解等。下列各组混和物的分离或提纯应采用什么方法?
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
(2)用CCl4提取溴水中的溴,可采用的方法。
(3)粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐。对粗盐中的这些杂质可采用和的方法除去。
(4)除去氧化钙中的碳酸钙可用的方法。
现有①铁片 ②NaCl溶液③氨水④醋酸⑤酒精⑥盐酸 ⑦H2SO4
⑧KOH固体 ⑨蔗糖 ⑩KAl(SO4)2·12H2O,其中能导电的是,属于电解质的是_______,属于非电解质的是,属于酸的是,属于碱的是。(填序号)
美国化学家R.F.Heck因发现如下Heck反应而获得2010年诺贝尔化学奖。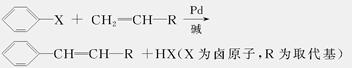

回答下列问题:
(1)C与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,F的结构简式______。D在一定条件下反应生
成高分子化合物G,G的结构简式是___________________________。
(2)在A→B的反应中,检验A是否反应完全的试剂是_______________________________。
(3)E的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为_________________________________________________________________________。