阿伏加德罗常数约为6.02×1023 mol-1,下列叙述中正确的是( )
| A.1.01×105 Pa、25 ℃时,2.24 L Cl2中含有的原子数为0.2×6.02×1023 |
| B.0.1 L 3 mol·L-1 NH4NO3溶液中含有的N原子数目为0.3×6.02×1023 |
| C.5.6 g铁粉与足量CuSO4溶液反应生成的铜原子数为1×6.02×1023 |
| D.46 g NO2和N2O4的混合物中含有的原子数为3×6.02×1023 |
下列叙述中,错误的是
| A.原子半径 Cl>S>O | B.还原性 Na>Mg>Al |
| C.稳定性 HF>HCl>HBr | D.酸性 HClO4>H2SO4>H3PO4 |
X元素的阳离子和Y元素阴离子具有与氩原子相同的电子层结构,下列叙述正确的是
| A.X的原子序数比Y的小 | B.X原子的最外层电子数比Y的多 |
| C.X的离子半径比Y的大 | D.X的原子半径比Y的大 |
下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是
| A.10与12 | B.8与17 | C.19与17 | D.6与14 |
下列化学用语,不正确的是
A.氮分子的电子式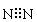 |
B.氯原子的结构示意图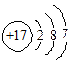 |
C.Na2S的电子式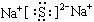 |
D.水分子的结构式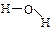 |
乙二酸(HOOC—COOH)可以被强氧化剂氧化为CO2,现有0.10mol/L乙二酸溶液20mL,恰好被4×10-3molVO2+所氧化,则此反应的还原产物VOn+中n的值为
| A.5 | B.4 | C.3 | D.2 |