某混合气体可能含有N2、HCl和CO,把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体的体积都没有变化。再通过足量的Na2O2固体,气体体积减小。最后通过灼热的铜网,经充分反应后气体体积又减小,但还有剩余气体。以下对混合气体组成的判断,正确的是
| A.一定没有N2,CO和HCl中至少有一种 | B.一定有N2、HCl和CO |
| C.一定有N2,CO和HCl中至少有一种 | D.一定有N2和HCl,没有CO |
已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H=74.9kJ·mol-1,下列说法中正确的是()
△H=74.9kJ·mol-1,下列说法中正确的是()
| A.该反应中熵变、焓变皆大于0 |
| B.该反应是吸热反应,因此一定不能自发进行 |
| C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
25℃、101kPa下:①2Na(s)+ O2(g)=Na2O(s) △H = -414kJ·mol-1
O2(g)=Na2O(s) △H = -414kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s) △H = -511kJ·mol-1
下列说法正确的是()
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25℃、101kPa下:Na2O2(s)+2Na(s)=2Na2O(s) △H = -317kJ·mol-1 |
高温下,某反应达到平衡,平衡常数K=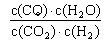 。恒容时,温度升高,H2浓度减小。下列说法正确的是()
。恒容时,温度升高,H2浓度减小。下列说法正确的是()
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO+H2O CO2+H2 CO2+H2 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O,根据此反应判断下列叙述中正确的是()
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb+SO42--2e–=PbSO4 |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
能够使反应Cu+2H2O=Cu(OH)2+ H2↑发生的是()
| A.用铜片作阴、阳极,电解氯化铜溶液 |
| B.用铜片作阴、阳极,电解硫酸钾溶液 |
| C.铜锌合金在潮湿空气中发生电化学腐蚀 |
| D.铜片和碳棒用导线相连后同时插入一烧杯内的氯化钠溶液中 |