人教版新课标化学教材九年级上册(2012教育部审定)“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 |
实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 |
A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 |
试管中均产生气泡,带火星木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 |
|
| Ⅳ分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
|
【实验结论】(1)A中产生的气体是 ;
(2)实验Ⅱ、Ⅲ证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)写出氧化铁和过氧化氢反应的符号表达式 。
【实验评价】 (1)实验设计Ⅳ的目的是 ;
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
【实验拓展】
查阅资料得知,CuO、CuSO4、、、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。
下列有关催化剂的说法中正确的是 。
A、MnO2只能作过氧化氢溶液分解的催化剂
B、同一个化学反应可以有多种催化剂
催化剂只能加快化学反应的速率
D、用作催化剂的物质不可能是其他反应的反应物或生成物
(1)学习二氧化碳性质时,老师做了如右图所示的实验。结果发现,澄清石灰水变浑浊。请写出澄清石灰水变浑浊有关反应的化学方程式_____________________。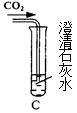
老师提出:氢氧化钠与氢氧化钙同属于碱类化合物,与氢氧化钙的化学性质相似,那么,氢氧化钠能否与二氧化碳反应呢?
同学们围绕着这个问题,通过查阅资料得知:常温下,CO2+2NaOH=Na2CO3+H2O。
接着,在老师指导下,完成了如下实验:将上述实验中的澄清石灰水换成氢氧化钠溶液,向其中通入CO2,观察到的实验现象为_________________________。
(2)为了验证CO2能与氢氧化钠发生化学反应,同学们设计了如下实验
①甲实验:向盛满CO2的塑料矿泉水瓶(质软)中加入一定量NaOH溶液,迅速旋紧瓶塞,并振荡。静止一会儿后观察到的实验现象为________________________。
②乙实验:向盛满CO2的集气瓶中倒入一定量NaOH溶液,迅速在瓶口处塞上一个去壳熟鸡蛋,静止一会儿后可观察到的实验现象为________________________。
(3)做完上述实验后,部分同学提出质疑,认为上述实验不足以说明CO2与氢氧化钠发生了化学反应。你认为这部分同学提出上述质疑,主要考虑的干扰因素是________________。为了进一步验证CO2能与氢氧化钠发生化学反应,同学们又设计了如下实验:
①A瓶盛装的试剂是________________,B瓶盛装的试剂是______________,实验时应_____
[填“打开”或“关闭”]活塞K。
②进行此实验时,通入CO2的体积应__________[填“大于”、“等于”或“小于”]A瓶溶液的体积。
③能证明CO2能与氢氧化钠发生化学反应的实验现象是______________________________。
(5分)维生素C(简称Vc,又名抗坏血酸),易溶于水,易被氧化。人体缺乏Vc可能引发多种疾病。水果和蔬菜中含有丰富的Vc。某研究性学习小组对它探究如下:
探究一:测定新买的饮料中Vc的含量。
【查阅资料】Vc能和高锰酸钾反应,使紫色的高锰酸钾溶液褪色。
【设计方案】分别向盛有lmL等浓度高锰酸钾稀溶液的四只试管中逐滴滴加新买的果味饮料、苹果汁、梨汁和新配制的0.04%的Vc溶液,边滴边振荡,直至高锰酸钾溶液褪色。
【实验数据】 
【实验结论】分析数据可知,新买的饮料中Vc含量最高的是,含量为
(各液体密度上的差别忽略不计)。
探究二:蔬菜放置时间的长短对其Vc含量是否有影响。
【设计方案】请你用新鲜的黄瓜、放置一周的黄瓜、高锰酸钾稀溶液和必要的仪器设计实验方案:。
【实验结论】按上述方案实验,根据这一实验结果,分析得出蔬菜放置时间的长短对其Vc的含量有影响。
【实验反思】对比实验需要控制变量。在做探究二时,下列情况影响到测定结果的是。
A.量取的高锰酸钾溶液的体积不同
B.新鲜黄瓜汁是其他班级用剩下的,而放置一周的黄瓜汁是当时榨的
C.没有用同一规格胶头滴管滴加
小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动。
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液……
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液……
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。(填表中空格)
| 实验一 |
实验二 |
实验三 |
|
实验 方案 |
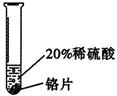 |
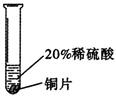 |
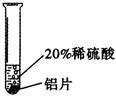 |
| 实验 现象 |
铬片表面产生气泡缓慢,溶液变蓝色。 |
___________________ |
铝片表面产生气泡较快。 |
| 结论 |
铬能和稀硫酸发生反应,反应速率较慢。 |
铜不与稀硫酸反应 |
_____________________ |
| 三种金属在金属活动性顺序中的相对位置关系是__________________________ |
【回答问题】
(1)用砂纸打磨金属片的目的是_____________________。
(2)实验一所发生反应的化学方程式是____________________________。
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是__________________。
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是________________。
【归纳】比较金属活动性强弱的方法有_____________(写一种即可)。
某兴趣小组话动中,在空气中点燃镁条时,发现在生成的白色固体物质中夹杂着少量的淡黄色固体。为了探究其原因,小组成员进行了以下探究活动:
[提出问题] 淡黄色固体物质的成分是什么?
[查阅资料] 通过查阅资料,记录了下列几种物质的颜色:
| 物 质 |
MgO |
MgCl2 |
Mg3N2 |
Mg(NO3)2 |
MgCO3 |
Mg(OH)2 |
| 颜 色 |
白色 |
白色 |
淡黄色 |
白色 |
白色 |
白色 |
小组成员一致认为产物中一定不含有氯化镁,理由是。
[提出猜想] 淡黄色的固体可能是。(填化学式)
[实验探究](1)按下图所示装置收集氮气(关闭a、b、c,用凸透镜聚光引燃白磷,待白磷不再燃烧并冷却至室温后,打开a、b,使用打气筒进行充气至A中的水进入B时,打开c,继续充气。)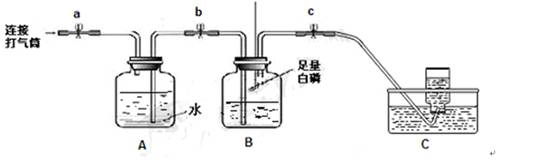
(2)实验验证的方法是
。
[实验结论] 猜想是正确的。镁条在空气中燃烧的有关化学反应方程式是
。
[实验反思] (1)氮气选用排水法收集的原因是。
(2)本探究活动对物质燃烧新的认识是。
小明买了一种“汽泡爽”的冲调饮料。
【饮料说明】
①主要原料:柠檬酸(C6H8O7)和小苏打(NaHCO3);
②使用说明:将一包“汽泡爽”粉末倒入玻璃杯中,加入200 mL冷水,看到有大量气泡快速生成,待粉末完全溶解,就得到一杯果味饮料。
小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响。
【实验一】探究“汽泡爽”产生气体的成分。
(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,填写生成气体的化学式。
3NaHCO3 + C6H8O7 ="===" C6H5O7Na3 + 3H2O + 3↑
(2)为了检验该气体,小明选择的试剂是。
【实验二】探究加水温度对产生气体量的影响。
(1)小明先用冷水和热水各冲了一杯饮料,品尝时发现冷水冲的饮料中气泡较多,热水冲的饮料中气泡较少。当他摇动杯子时,发现有大量气泡从水中逸出。他查阅资料发现:随着温度升高,气体在一定量的水中溶解的量会迅速降低。于是小明设计了如下实验方案,请填写表中空白。
| 实验序号 |
加入水的体积 |
加入水的温度 |
收集到的气体的体积 |
| 1 |
200 mL |
15℃ |
a(待记录) |
| 2 |
50℃ |
b(待记录) |
(2)在老师的帮助下,小明采用相同的两套实验装置(如下图)分别完成上述实验,在A中加入水,再加入一袋“汽泡爽”,迅速塞紧胶塞。量筒C用于收集A中产生的气体所排出的液体,冷却至室温后读取数据。B中油层的作用是。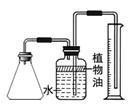
A B C
(3)通过实验,小明测得:a =" 64" mL,b =" 132" mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系。但是老师看到小明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的总量应该近似相等,与温度关系不大,其本质原因是。
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是。