电解法制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42—杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下: 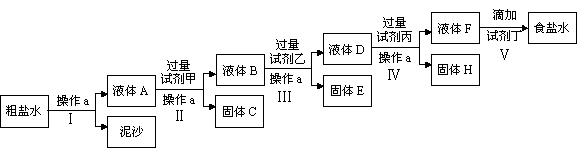
请回答以下问题:
(1)操作a的名称是_______,所用玻璃仪器有____________、玻璃棒、烧杯;
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的难溶沉淀,则试剂甲为(填化学式)____溶液;
(3)写出固体H所含物质的化学式_____________;
(4)在Ⅴ步中,逐滴加入试剂丁直至溶液无明显变化时,写出此过程中发生反应的离子方程式: _______________________;_______________________。
下列说法正确的是
| A.使紫色石蕊试液变红的溶液中:Fe2+、Cu2+、Cl-、NO3-能够大量共存 |
| B.加入铝粉放出H2的溶液中:Na+、Mg2+、HCO3-、SO42-不能大量共存 |
| C.常温下,醋酸钠与醋酸的混合液PH=7:则c(Na+)= c(CH3COO-) |
| D.0.1mol/L NaHCO3溶液中:c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3) |
图中a、b、c、d、e、f表示元素周期表中部分短周期元素,下列叙述正确的是
| A.a、b、c的简单离子中,的离子半径最大 |
| B.c、d、f最高价氧化物对应的水化物两两之间均可发生反应 |
| C.e的氢化物比f的氢化物的稳定性高 |
| D.a、e可形成一种新型无机非金属材料——高温结构陶瓷 |
下列实验不能达到预期目的的是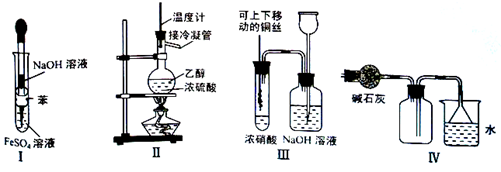
| A.利用Ⅰ制取Fe(OH)2 |
| B.利用Ⅱ装置制取C2H4 |
| C.利用Ⅲ装置进行铜与浓硝酸反应的实验 |
| D.利用Ⅳ装置收集NH3 |
下列类比关系正确的是
| A.AlCl3与过量NaOH溶液反应生成AlO2-,则与过量NH3·H2O也生成AlO2- |
| B.Na2O2与CO2反应生成Na2CO3和O2,则与SO2反应可生成Na2SO3和O2 |
| C.Fe与Cl2反应生成FeCl3,则与I2反应可生成FeI3 |
| D.Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应 |
设nA为阿伏加德罗常数的数值,下列说法错误的是
| A.1molNH3中含有3nA个N-H键 |
| B.0.1mol/L Na2CO3溶液中含有0.1nA个CO32- |
| C.标准状况下,11.2L CO2中含有nA个O原子 |
D.20g重水( )中含有10nA个个电子 )中含有10nA个个电子 |