高铁酸钾(K2FeO4)是一种高效绿色水处理剂,其工业制备的反应原理为:2Fe(OH)3 +3KClO+4KOH=2K2FeO4+3KCl+5H2O ,下列说法正确的是
| A.制高铁酸钾用 KClO做还原剂 |
| B.KCl是还原产物 |
| C.高铁酸钾中铁的化合价为 +7 |
| D.制备高铁酸钾时1 molFe(OH)3得到3 mol电子 |
"化学,让生活更美好",下列叙述不能直接体现这一主旨的是
| A. | 风力发电,让能源更清洁 | B. | 合成光纤,让通讯更快捷 |
| C. | 合成药物,让人类更健康 | D. | 环保涂料,让环境更宜居 |
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知
、
和
的燃烧热
分别为-285.8
、-283.0
和-726.5
。请回答下列问题:
(1)用太阳能分解10
水消耗的能量是
;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为;
(3)在溶积为2
的密闭容器中,由
和
合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:
均大于300℃);
下列说法正确的是(填序号)
温度为
时,从反应开始到平衡,生成甲醇的平均速率为
②该反应在
时的平衡常数比时的小
③该反应为放热反应
④处于
点的反应体系从
变到
,达到平衡时
增大
(4)在
温度时,将1
和3
充入一密闭恒容器中,充分反应达到平衡后,若
转化率为
,则容器内的压强与起始压强之比为;
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为、正极的反应式为。理想状态下,该燃料电池消耗1
甲醇所能产生的最大电能为702.1
,则该燃料电池的理论效率为(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)
0.80
•5
样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
请回答下列问题:
(1)试确定200℃时固体物质的化学式(要求写出推断过程);
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为。把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为,其存在的最高温度是;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与
在加热时发生反应的化学方程式为;
(4)在0.10
·
硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的
=8时,
(
)=
·
(
[
]=2.2×10-20)。
若在0.1
·
硫酸铜溶液中通入过量
气体,使
完全沉淀为
,此时溶液中的
浓度是
·
。
能正确表示下列反应的离子方程式为()
| A. |
硫化亚铁溶于稀硝酸中:
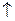
|
| B. | 溶于过量的 溶液中: |
| C. | 少量 通入苯酚钠溶液中: |
| D. |
大理石溶于醋酸中:
+
=
+
+
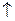 + +
|
铁镍蓄电池又称爱迪生电池,放电时的总反应为: 下列有关该电池的说法不正确的是()
| A. | 电池的电解液为碱性溶液,正极为 、负极为 |
| B. | 电池放电时,负极反应为 |
| C. | 电池充电过程中,阴极附近溶液的 降低 |
| D. | 电池充电时,阳极反应为 |