下列实验操作正确的是( )
| A.蒸馏操作时,应使温度计水银球插入蒸馏烧瓶的溶液中 |
| B.过滤操作时,玻璃棒应靠在三层滤纸的一侧 |
| C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| D.分液操作时,分液漏斗中下层液体从下口放出,上层液体也从下口放出 |
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是
| A.原子半径的大小顺序:r(Y)>r(Z)>r(W) |
| B.元素Z、W的简单离子的电子层结构不同 |
| C.元素Y的简单气态氢化物的热稳定性比Z的强 |
| D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
下列叙述正确的是
| A.乙酸与丙二酸互为同系物 |
| B.不同元素的原子构成的分子只含极性共价键 |
C.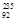 U和 U和 U是中子数不同质子数相同的同种核素 U是中子数不同质子数相同的同种核素 |
| D.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
| A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 |
| B.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
| C.元素X不能与元素Y形成化合物X2Y2 |
| D.元素W、R的最高价氧化物的水化物都是强酸 |
科学研究证明:核外电子的能量不仅与电子所处的能层、能级有关,还与核外电子数目及核电荷的数目有关。氩原子与硫离子的核外电子排布相同,都是1s22s22p63s23p6。下列说法正确的是
| A.两粒子的1s能级上电子的能量相同 |
| B.两粒子的3p能级上的电子离核的距离相同 |
| C.两粒子的电子发生跃迁时,产生的光谱不同 |
| D.两粒子都达8电子稳定结构,化学性质相同 |
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同电子层结构,则下列叙述正确的是
| A.原子半径A>B>D>C | B.原子序数d>c>b>a |
| C.离子半径C>D>B>A | D.单质的还原性A>B>D>C |