在MgSO4和Al2(SO4)3的混合溶液中,测得Mg2+物质的量浓度为0.1mol/L,
物质的量浓度为0.4mol/L,则混合溶液中Al3+物质的量的浓度为( )
| A.0.2mol/L | B.0.15mol/L | C.0.1mol/L | D.0.05mol/L |
相同温度下,两个恒压密闭容器中发生可逆反应X2(g)+3Y2(g) 2XY3(g) ΔH=-92.6kJ·mol-1实验测得反应在起始及达到平衡时的有关数据如下表所示:
2XY3(g) ΔH=-92.6kJ·mol-1实验测得反应在起始及达到平衡时的有关数据如下表所示:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡时体系能量变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
0.1 |
0.3 |
0 |
4.63kJ |
| ② |
0.8 |
2.4 |
0.4 |
Q(Q>0)kJ |
下列叙述正确的是
A.反应的平衡常数:①>②
B.达平衡时,两个容器中XY3的物质的量浓度均为2mol·L-1
C.达到平衡时,容器①、②中各物质的百分含量相同
D.若容器①体积为0.20L,则达平衡时放出的热量大于4.63kJ
以NA代表阿伏加德罗常数,有关反应:C2H2(g)+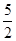 O2(g)→2CO2(g)+H2O(1);ΔH=-1300kJ/mol。下列关于热化学方程式的说法正确的是
O2(g)→2CO2(g)+H2O(1);ΔH=-1300kJ/mol。下列关于热化学方程式的说法正确的是
| A.有10NA个电子转移时,该反应放出1300kJ的能量 |
| B.有NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C.有4NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D.有8NA个碳氧共用电子对生成时,吸收1300kJ的能量 |
可逆反应A(g)+3B(g) 2C(g);ΔH=-Q kJ/mol。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1 kJ在相同的条件下,向乙容器中加入2mol C达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是
2C(g);ΔH=-Q kJ/mol。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1 kJ在相同的条件下,向乙容器中加入2mol C达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是
A.甲中A的转化率为75%
B.Q1+Q2=Q
C.达到平衡后,再向乙中加入0.25 molA、0.75molB 、1.5molC,平衡向正反应方向移动
D.乙中的热化学反应方程式为2C(g) aA(g)+3B(g);ΔH=+Q2kJ·mol-1
aA(g)+3B(g);ΔH=+Q2kJ·mol-1
已知可逆反应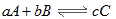 中,A、C的含量随温度的变化曲线如图所示,下列说法正确的是
中,A、C的含量随温度的变化曲线如图所示,下列说法正确的是
A.该反应在T1、T3温度时达到过化学平衡
B.该反应在T2温度时达到过化学平衡
C.该反应的正反应是吸热反应
D.升高温度,平衡会向正反应方向移动
工业制A1,你认为说法不妥当的是
| A.铝便于运输、贮存,从安全角度考虑,铝是最佳燃料之一 |
| B.铝资源比较丰富,易于开采,且可以再生 |
| C.铝燃烧热大,燃烧污染小,易有效控制 |
| D.寻找高效催化剂,使A12O3分解同时释放能量,是铝能源大规模开发利用的一项关键技术 |