能用离子方程式“Ba2+ +SO42—==BaSO4↓”表示的化学反应是
| A.Ba(OH)2+H2SO4==BaSO4↓+2H2O |
| B.Na2CO3+H2SO4==Na2SO4+H2O+CO2↑ |
| C.BaCl2+H2SO4==BaSO4↓+2HCl |
| D.Zn+H2SO4==ZnSO4+H2↑ |
室温下,在0.2mol/L
溶液中,逐滴加入1.0mol/L
溶液,实验测得溶液pH随
溶液体积变化曲线如下图,下列有关说法正确的是()
| A. |
a点时,溶液呈酸性的原因是
水解,离子方程式为:
|
| B. | a→b段,溶液pH增大, 浓度不变 |
| C. | b→c段,加入的OH -主要用于生成 沉淀 |
| D. | d点时, 沉淀开始溶解 |
中学化学中很多"规律"都有适用范围,下列根据有关"规律"推出的结论正确的是()
选项 规律 结论
| A. |
A 较强酸可以制取较弱酸 次氯酸溶液无法制取盐酸 |
| B. |
B 反应物浓度越大,反应速率越快 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C. |
C 结构和组成相似的物质,沸点随 NH3沸点低于PH3 相对分子质量增大而升高 |
| D. |
D 溶解度小的沉淀易向溶解度更小 ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 的沉淀转化 |
室温下,下列溶液中粒子浓度大小关系正确的是
| A. | 溶液: |
| B. | 溶液中: |
| C. | 溶液: |
| D. | 和 混合溶液: |
臭氧是理想的烟气脱硝剂,其脱硝反应为:
 ,反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
,反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是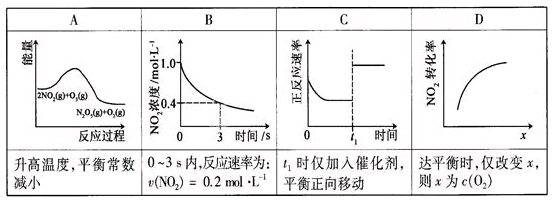
为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是
| 选项 |
实验目的 |
主要仪器 |
试剂 |
| A |
分离
和
混合物 |
分液漏斗、烧杯 |
和
混合物、蒸馏水 |
| B |
鉴别葡萄糖和蔗糖 |
试管、烧杯、酒精灯 |
葡萄糖溶液、蔗糖溶液、银氨溶液 |
| C |
实验室制取 | 试管、带导管的橡皮塞 |
锌粒、稀 |
| D |
测定
溶液浓度 |
滴定管、锥形瓶、烧杯 |
溶液,0.1000
盐酸 |