CH4、H2、CO的燃烧热分别为890.31kJ/mol、285.8kJ/mol、110.5 kJ/mol,下列热化学方程式书写正确的是
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-890.31kJ/mol |
| B.2H2(g)+ O2(g)= 2H2O(l)ΔH=-285.8kJ/mol |
| C.CO (g)+ H2O(g)= CO2(g)+ H2 (g)ΔH=+175.3kJ/mol |
| D.2CO (g)+ O2(g) = 2CO2(g)ΔH="-221" kJ/mol |
科学家最近发现两种粒子;第一种是只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”,第二种是由四个氧原子构成的分子,下列有关这两种粒子的说法不正确的是
| A.“四中子”不显电性 |
| B.“四中子”的质量数为4,其质量比氢原子大 |
| C.第二种粒子是氧元素的另一种同位素 |
| D.第二种粒子的化学式为O4,与O2互为同素异形体 |
氨跟氧化铜反应可以制备氮气2 NH3+3CuO
NH3+3CuO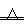


缓冲溶液可以抗御少量酸碱对溶液pH的影响。人体血液量最主要的缓冲体系是碳酸氢盐缓冲体系(H2CO3/HCO3-),维持血液的pH稳定。已知在人体正常体温时,反应H2CO3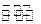 HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,1g2=0.3。则下列判断正确的是()
HCO3-+H+的Ka=10-6.1,正常人的血液中c(HCO3-):c(H2CO3)≈20:1,1g2=0.3。则下列判断正确的是()
| A.正常人血液内Kw=10-14 |
B.由题给数据可算得正常人血液的pH约为7.4 |
| C.正常人血液中存在:c(HCO3-)+c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) | |
| D.当过量的碱进入血液中时,只有发生HCO3-+OH=CO32-+H2O的反应 |
下列离子方程式正确的是()
| A.少量的钠跟足量盐酸反应:2Na+2H2O=2Na++2OH-+H2↑ |
| B.过量Cl2通向湿润的淀粉KI试纸,先变蓝后褪去:Cl2+2I-=2Cl-+I2 |
| C.Ba(HCO3)2溶液与Ba(OH)2溶液任意比混合:Ba2++HCO3-+OH-=BaCO3↓+H2O |
D.向浓HNO3溶液中加入足量的 铁粉:Fe+2NO3-+4H+=Fe2++2NO2↑+2H2O 铁粉:Fe+2NO3-+4H+=Fe2++2NO2↑+2H2O |
下图是一种由苄叉丙酮合成肉桂酸的工业流程。下列有关说法正确的是()
| A.反应I的实质是有机物发生还原反应 |
| B.肉桂酸分子中的所有碳原子一定在同一平面上 |
C.苄叉丙酮在一定条件下可以合成高分子 化合物 化合物 |
| D.反应II先加入还原剂的目的是要还原反应体系中的有机物 |