浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是
| A.酸性 | B.脱水性 | C.强氧化性 | D.吸水性 |
下列有关说法正确的是
| A.反应NH3(g)+HCl(g)= NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀 |
| C.CH3COOH溶液加水稀释后,电离平衡正向移动,溶液中的c(CH3COO-)增大 |
| D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
下图两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是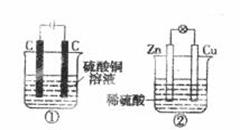
| A.产生气体体积:①=② |
| B.溶液的pH变化:①减小,②增大 |
| C.电极反应式:①中阳极为4OH--4e-=2H2O+O2↑②中负极为2H++2e-=H2↑ |
| D.①中阴极质量增加,②中正极质量减小 |
25℃时,水中存在电离平衡:H2O  H++OH- △H>0。下列叙述正确的是
H++OH- △H>0。下列叙述正确的是
| A.将水加热,KW增大,pH不变 |
| B.向水中加入少量NaHSO4固体,c(H+)增大,KW不变 |
| C.向水中加入少量NaOH固体,平衡逆向移动,c(OH-)降低 |
| D.向水中加入少量NH4Cl固体,平衡正向移动,c(OH-)增大 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温下,16gCH4含有10NA个电子 |
| B.标准状况下,22.4L苯含有NA个苯分子 |
| C.标准状况下,6.72LNO2与水充分反应转移的电子数目为0.1NA |
| D.0.1mol.L-1CH3COOH溶液中含有0.1NA个CH3COO- |
升高温度,下列数据不一定增大的是
A.化学反应速率 |
B.KNO3的溶解度S |
| C.化学平衡常数K | D.水的离子积常数KW |