下列评价合理的是( )
| 选项 |
化学反应及其离子方程式 |
评价 |
| A |
Fe3O4与稀硝酸反应:2 Fe3O4+18H+=6Fe3++H2↑+8H2O |
正确 |
| B |
向碳酸镁中加入稀盐酸: CO32—+2H+=CO2↑+H2O |
错误,碳酸镁不应写成离子形式 |
| C |
向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42—=BaSO4↓ |
正确 |
| D |
FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br—+2Cl2="2" Fe3++4Cl—+Br2 |
错误:Fe2+与Br—的化学计量数之比应为1:2 |
下列对某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO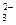 |
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不溶解,一定有CO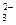 |
C.加入氢氧化钠并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH |
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白 色沉淀不溶解,一定有Ba2+ 色沉淀不溶解,一定有Ba2+ |
为提纯下列物质(括号中为杂质),所选除杂质试剂和分离方法都正确的是
| 选项 |
被提纯的物质(杂质) |
除杂试剂 |
分离方法 |
| A |
NH3(H2O) |
浓硫酸 |
洗气 |
| B |
乙酸乙酯(乙酸) |
饱和碳酸钠溶液 |
分液 |
| C |
KCl 固体(I2) 固体(I2) |
NaOH溶液 |
加热 |
| D |
苯(苯酚) |
浓溴水 |
过滤 |
下列是某同学在实验报告中记录的数据,其中正确的是
| A.用25 mL量筒量取12.36 mL盐酸 |
| B.用托盘天平称取8.75 g食盐 |
| C.用广泛pH试纸测得某溶液的pH为3.5 |
| D.用标准NaOH溶液滴定未知浓度的盐酸,用去NaOH溶液23.10 mL |
下列实验方法:①用渗析法分离蛋白质和葡萄糖的混合物②用盐析法分离油脂皂化反应产物③用升华法分离沙子和碘的混和物④用重结晶法分离硝酸钾和氯化钠的混合物⑤用分液法分离水和溴乙烷的混合物⑥用蒸馏法分离酒精与苯酚(沸点182℃)的混合物。下列选项正确的是
| A.只有①不正确 | B.②⑤⑥不正确 |
| C.只有③④⑥正确 | D.全部正确 |
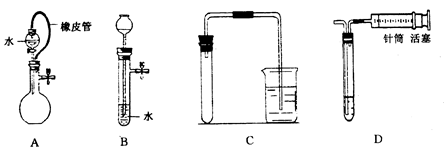
对下列装置,不添加其他仪器无法检查气密性的是