在通常条件下,下列各组物质的性质排列正确的是( )
| A.熔点:CO2>H2O2>SiO2 | B.酸性:HClO>H2SO3>H2CO3 |
| C.沸点:乙烷>戊烷>丁烷 | D.热稳定性:HF>H2O>NH3 |
一定能在下列溶液中大量共存的离子组是
①含有大量Al3+的溶液中:Na+、NH4+、SO42—、Cl-
②加入Al能放出H2的溶液中:Cl-、HCO3—、SO42—、NH4+
③含有大量Fe3+的溶液中:Na+、Mg2+、NO3—、SCN-
④在含有大量AlO2—的溶液中:NH4+、Na+、Cl-、H+
⑤由水电离出的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3—
| A.①② | B.①③⑤ | C.① | D.①④⑤ |
下列离子方程式不正确的是
| A.0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合: HSO3-+ClO-=SO42-+Cl-+H+ |
| B.氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| C.漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀: Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO |
| D.NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO42—恰好沉淀完全:NH4++H++SO42-+Ba2++2OH-=NH3·H2O+BaSO4↓+H2O |
用NA表示阿伏加德罗常数的数值,下列叙述正确的是
①0.84 g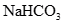 晶体中阴离子数为0.01NA
晶体中阴离子数为0.01NA
②常温下,1L0.1 mol·L-1 Na2CO3溶液中阴离子数目之和大于0.1 NA
③常温常压下,0.3molCl2通入水中,充分反应后转移电子数目为0.3 NA
④7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1 NA
⑤标准状况下,22.4LSO3的分子数为NA
⑥标准状况下,22.4LNO和11.2L O2混合后气体的分子总数等于NA
| A.①②③ | B.①②④ | C.②④⑥ | D.③④⑤ |
设NA为阿伏加德罗常数的值。下列说法不正确的是
| A.常温下,30 g的2-丙醇中含有羟基的数目为0.5 NA |
| B.15 g C2H6含C—H键数目为3NA |
| C.28 g乙烯与丙烯的混合气体,含碳原子总数为2NA |
D.7.8 g 中含有的碳碳双键数目为0.3NA 中含有的碳碳双键数目为0.3NA |
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径在36~55 nm的磁流体。下列说法中正确的是
| A.所得的分散系属于悬浊液 |
| B.该分散系能产生丁达尔效应 |
| C.所得的分散系中分散质为Fe2O3 |
| D.所得分散系为胶体,且胶粒直径即为氢氧化铁分子直径 |