某同学设计在KOH溶液中用铂作电极,利用CH3OH和O2的反应来构成原电池。下列说法正确的是( ):①正极上O2得到电子,发生还原反应②每消耗1molCH3OH可以向外电路提供6mole-③该电池的总反应为:2CH3OH+3O2=2CO2+4H2O④电池放电后,溶液的pH不断升高
| A.①② | B.①③ | C.②③ | D.③④ |
用铜、银和硝酸银溶液设计一个原电池,下列对该原电池的判断正确的是
| A.铜作负极被氧化 | B.银为正极被还原 |
| C.正极反应为:Ag+ + e-="Ag" | D.NO3-向正极移动 |
下列描述的过程中一定有新物质生成的是
| A.有热量吸收或有热量放出的变化 | B.石墨转换为金刚石 |
| C.有化学键断裂和形成的变化 | D.将含钠元素的物质在酒精灯火焰上灼烧 |
下列化学用语正确是
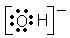
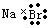
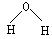
| A.Cl-的示意图 | B.OH-的电子式 | C.溴化钠的电子式 | D.水分子的结构式 |
氢化铵(NH4H)与氯化铵结构相似,又已知NH4H 与水反应有H2生成,下列叙述中正确的是
| A.NH4H是共价化合物 | B.NH4H溶于水后,所形成的溶液显酸性 |
| C.NH4H溶于水时,NH4H是氧化剂 | D.NH4H固体投入少量水中,有两种气体生成 |
元素X的原子核外M电子层上有3个电子,元素Y2-的离子核外有18个电子,则这两种元素可形成的化合物为
| A.XY2 | B.X2Y3 | C.X3Y2 | D.X2Y |