下列选项中,有关实验操作、现象和结论都正确的是( )
| 选项 |
实验操作 |
现象 |
结论 |
| A |
将过量的CO2通入CaCl2溶液中 |
无白色沉淀出现 |
生成的Ca(HCO3)2可溶于水 |
| B |
常温下将Al片插入浓硫酸中 |
无明显现象 |
Al片和浓硫酸不反应 |
| C |
向饱和Na2CO3溶液中通入足量CO2 |
溶液变浑浊 |
析出了NaHCO3 |
| D |
将SO2通入溴水中 |
溶液褪色 |
SO2具有漂白性 |
在密闭容器中发生反应:aX(g)+bY(g)  cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍,下列叙述中不正确的是
cZ(g)+dW(g),反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍,下列叙述中不正确的是
| A.平衡向逆反应方向移动 | B.a+b<c+d |
| C.Z的体积分数增加 | D.X的转化率下降 |
某温度下,在容积不变的密闭容器中存在下列可逆反应:A(g)+3B(g)  2C(g),达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则下列说法正确的是
2C(g),达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则下列说法正确的是
A.平衡不移动 B.平衡时C的物质的量增大
C.平衡向逆反应方向移动 D.平衡时混合气体的平均摩尔质量减少
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列说法正确的是 
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls) |
| B.反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始到10s时,Y的转化率为79.0% |
D.反应的化学方程式为: X(g)+Y(g)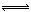 Z(g) Z(g) |
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸汽的物质的量增加了0.45mol,则此反应的平均速率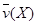 (反应物的消耗速率或产物的生成速率)可表示为
(反应物的消耗速率或产物的生成速率)可表示为
A.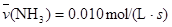 |
B.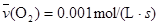 |
C.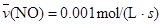 |
D.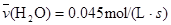 |
将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s) NH3(g)+HI(g);2HI(g)
NH3(g)+HI(g);2HI(g) H2(g)+I2(g),当反应达到平衡时,C(H2)=0.5mol/L,C(HI)=4mol/L,则第一个反应在该温度下的平衡常数是
H2(g)+I2(g),当反应达到平衡时,C(H2)=0.5mol/L,C(HI)=4mol/L,则第一个反应在该温度下的平衡常数是
| A.20 | B.15 | C.25 | D.16 |