某溶液可能含有Cl-、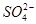 、
、 、NH+ 4、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
、NH+ 4、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
| A.NH+ 4Fe3+一定存在, K+可能存在 |
| B.Cl−一定存在,且c(Cl−)≤0.4 mol/L |
C.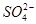 、NH+ 4Fe3+一定存在,且物质的量浓度均为0.02 mol/L 、NH+ 4Fe3+一定存在,且物质的量浓度均为0.02 mol/L |
D. 、Al3+一定不存在,K+一定存在 、Al3+一定不存在,K+一定存在 |
下列有关化学用语表示正确的是x k b 1 . c o m
| A.二氧化硅的分子式 SiO2 | B.氧化铁的化学式:FeO |
C.次氯酸的电子式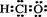 |
D.质子数为53,中子数为78的碘原子: |
下列有关实验的叙述,正确的是(填序号)
A用胶头滴管向试管中滴加液体,滴管一定不能伸入到试管中
B用渗析法分离淀粉中混有的NaCl杂质
C无法用分液漏斗将甘油和水的混合液体分离
D用酸式滴定管量取20.00mL高锰酸钾溶液
E.为了测定某溶液的pH,将未经湿润的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比
F.用浓氨水洗涤做过银镜反应的试管
G.配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
H.浓硫酸不小心沾到皮肤上,立刻用稀NaOH溶液洗涤
J.在氢氧化铁胶体中加入少量硫酸会产生沉淀
K.用结晶法可以除去硝酸钾中混有的少量氯化钠
按下图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体可能是()
| A.H2 | B.CO和H2 | C.NH3 | D.CH3CH2OH(气) |
某有机物的结构简式为: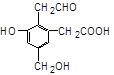
等物质的量的该物质分别与足量的Na、NaOH、新制Cu(OH)2反应,则需三种物质的物质的量之比为
| A.6∶4∶5 | B.1∶1∶1 | C.3∶2∶2 | D.3∶2∶3 |
以NA表示阿伏加德罗常数,下列说法正确的是()
| A.如果5.6L N2含有n个氮分子,则阿伏加德罗常数一定约为4n |
| B.15.6g Na2O2与过量CO2反应时,转移的电子数为0.2NA |
| C.1L 1mol/L 的FeCl3溶液中含有铁离子的数目为NA |
| D.1mol的甲烷中含有的C—H共价键的数目为6NA |