下列关于价电子构型3s23p4的描述正确的是
| A.它的元素符号为O |
| B.它的核外电子排布式为1s22s22p63s23p4 |
| C.可以与H2化合生成液态化合物 |
D.其轨道表示式为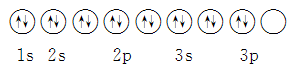 |
在密闭容器中进行如下反应:X2(g)+Y2(g)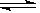 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A.Z为0.3 mol·L-1 | B.Y2为0.35 mol·L-1 |
| C.X2为0.2 mol·L-1 | D.Z为0.4 mol·L-1 |
某温度下,在一容积可变的容器中,反应2A(g)+ B (g) 2C(g)达到平衡时,A、B和C的物质的量分别是4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下处理,可使平衡右移的是()
2C(g)达到平衡时,A、B和C的物质的量分别是4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下处理,可使平衡右移的是()
A、均减半 B、均加倍 C、均增加1mol D均减少1mol
在10 ℃时,某化学反应速率为0.1 mol·L-1·s-1,若温度每升高10 ℃,反应速率增加到原来的2倍。为了把该反应速率提高到1.6 mol·L-1·s-1,则该反应需在什么温度下进行( )
| A.30 ℃ | B.40 ℃ | C.50 ℃ | D.60 ℃ |
如右图中的曲线是表示其他条件一定时,2NO+O2 2NO2(正反应是放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )
2NO2(正反应是放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )
| A.a | B.b | C.c | D.d |
已知:H2(g) + I2(g) 2HI(g)的平衡常数为K1;1/2 H2(g)+ 1/2 I2(g)
2HI(g)的平衡常数为K1;1/2 H2(g)+ 1/2 I2(g) HI(g)的平衡常数为K2,则K1、K2的关系为()。
HI(g)的平衡常数为K2,则K1、K2的关系为()。
| A.K1= 2K2 | B.K1= K22 | C.K1 = K2 | D.2K1= K2 |