在同温同压下,下列各组热化学方程式中,△H2>△H 1的是
| A.2H2(g)+O2(g)=2H2O(g) △H1;2H2(g)+O2(g)=2H2O(l)△H2 |
| B.S(g)+O2(g)=SO2(g)△H1;S(s)+O2(g)=SO2(g)△H2 |
| C.1/2C(s)+O2(g)=CO(g)△H1;C(s)+O2(g)=CO2(g)△H2 |
| D.HCl(g)=1/2 H2(g)+1/2 Cl2(g)△H1; H2(g)+Cl2(g)=2HCl(g)△H2 |
化学与生活生产、环境保护、资源利用、能源开发等密切相关。下列说法不正确的是
| A.实施“雨污分流”工程,可提高水资源的利用率 |
| B.煤的气化、液化是使煤变成清洁能源的有效途径 |
| C.垃圾分类有利于资源回收利用,废易拉罐属不可再生废物 |
| D.合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示。下列判断正确的是
| A.原溶液中一定含有Na2SO4 |
| B.原溶液中一定含有的阴离子是OH-,CO32-,SiO32-,AlO2- |
| C.反应后形成的溶液溶质为NaCl |
| D.原溶液中含有CO32-与AlO2-的物质的量比为1:2 |
将7.8g镁铝合金完全溶于适量的稀硫酸,产生标准状况下的气体8.96L,在所得溶液中加入足量的稀氨水,过滤,洗涤,将滤渣充分灼烧所得固体质量为
| A.14.2g | B.21.4g | C.5.8g | D.4g |
下列说法不正确的是
| A.Na2O2晶体中阴离子和阳离子的数目之比为1:2 |
| B.同温同压下等质量的N2和CO两种气体的体积比为1:1 |
| C.同温同压下,相同体积的O2和O3两种气体中的氧原子个数比为1:1 |
| D.等质量的乙烯和环己烷所含质子数比为1:1 |
X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如下图所示。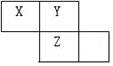
若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是
| A.Z的氧化物对应的水化物一定是一种强酸 |
| B.原子半径大小顺序是X>Y>Z |
| C.Z单质与Fe反应形成的化合物中,铁元素显+3价 |
| D.Y的单质比Z的单质更易与氢气反应 |