A、B、C、D是四种短周期元素,它们的原子序数依次增大。其中A、D元素同主族,B、C元素同周期;由A、B、C、D中的两种元素可形成原子个数比为1:1的多种化合物,甲、乙、丙、丁为其中的四种,它们的元素组成如下表所示: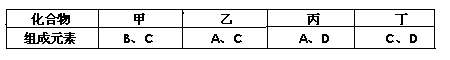
常温下,甲物质为气体,密度略小于空气;乙物质为液体;丙物质和丁物质为固体且都为离子化合物。请填写下列空白:
(1)D元素形成的简单离子的结构示意图为 ,丙物质的化学式为 ,丁物质中阴离子与阳离子的个数之比为 。
(2)若标准状况下5.6L甲物质完全燃烧放出的热量为QKJ,试写出表示甲物质燃烧热的热化学方程式 。
(3)研究表明乙物质具有弱酸性,则乙物质在水中的电离方程式为 。
(4)B、C两种元素按原子个数比为1:2可形成化合物戊,A、C、D三种元素按原子个数比为1:1:1可形成化合物己,则戊与己按物质的量3:4反应后溶液中溶质为 。
(5)某同学设计了一个以结构简式是BA3-CA物质为燃料的电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如下: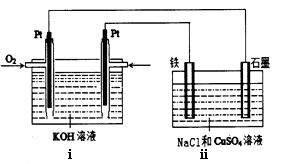
①写出ⅰ中通入该物质这一极的电极反应式 。
②理论上ⅱ中两极所得气体的体积随时间变化的关系如坐标图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式 ;在t2时所得溶液的H+ 浓度约为 。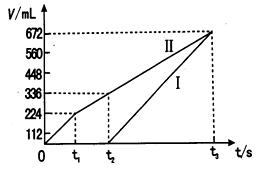
(10分,每空2分)水的电离平衡曲线如图所示。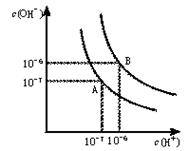
(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从增加到。
(2)将pH=8的NaOH溶液与pH=5的稀盐酸混合,并且保持100℃的恒温,欲使混合溶液pH=7,则NaOH与盐酸的体积比为。
(3)普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是。
(4)室温时,Mg(OH)2(S) Mg2+(aq)+2OH-(aq) 当Mg2+沉淀完全 (指Mg2+的浓度等于10-5mol/L) 时,溶液的pH=_______。已知25℃时Ksp[Mg(OH)2]=1.0×10-11,
Mg2+(aq)+2OH-(aq) 当Mg2+沉淀完全 (指Mg2+的浓度等于10-5mol/L) 时,溶液的pH=_______。已知25℃时Ksp[Mg(OH)2]=1.0×10-11,
(10分每空2分)室温下,在一个容积为1L的密闭容器中,充入1molN2和3molH2,发生反应:N2+3H2 2NH3,5min后到达平衡,平衡后混合气体的压强为起始压强的3\4,此时放出的热量为42KJ,则:
2NH3,5min后到达平衡,平衡后混合气体的压强为起始压强的3\4,此时放出的热量为42KJ,则:
(1)平衡时N2的物质的量为mol
(2)5min内用H2表示的反应速率为mol/(L.min)
(3)若向该1L密闭容器中再充入1molN2,则H2的转化率(填变大、变小或不变)
(4)写出N2和H2反应生成NH3的热化学反应方程式:
(5)写出该反应的平衡常数的表达式:
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO (g) + 2H2 (g)  CH3OH (g)△H=-116kJ/mol
CH3OH (g)△H=-116kJ/mol
(1)该反应的化学平衡常数表达式为;
(2)下列措施中有利于增大该反应的反应速率且提高转化率的是(填字母序号) 。
a.随时将CH3OH与反应混合物分离b.降低反应温度
c.使用高效催化剂 d.增大体系压强
(3)一定条件下,将1 mol CO与3 mol H2的混合气体在催化剂作用下发生反应生成甲醇,平衡后将容器的容积压缩到原来的l/2,其他条件不变,对平衡体系产生的影响是(填字母序号).
a.c ( H2 )减少
b.正反应速率加快,逆反应速率减慢
c.CH3OH 的物质的量增加
d.重新平衡c ( H2 )/ c (CH3OH )减小
(4)在密闭容器中充有1mol CO与2 mol H2,在催化剂作用下反应生成甲醇,CO的转化率(α)与温度(T)、压强(P)的关系如图所示。
①A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间,tAtC(填于“大于”、“小于”或“等于”)。
②若A点时容器的体积为1 L,该温度下B点的平衡常数K= 。
现有反应:mA(g)+ B(g) 2C(g),达到平衡后,当升高温度时,A的转化率变小;当减小压强时,混合体系中C的质量分数不变,则:
2C(g),达到平衡后,当升高温度时,A的转化率变小;当减小压强时,混合体系中C的质量分数不变,则:
(1)该反应的△H0(填“>”或“<”),且m1(填“>”“=”“<”)。
(2)若加入B(假设容器的体积不变),则A的转化率,B的转化率。(填“增大”“减小”或“不变”)
(3)若B是有色物质,A、C均无色,则加入C(假设容器的体积不变)时混合物颜色,
若维持容器内压强不变,充入氖气时,混合物颜色(填“变深”“变浅”或“不变”)。
(4)一定温度下,向1L密闭容器中加入1mol C(g)使其分解,气体A的物质的量随时间的变化如下图所示。
则0~2 min内的平均反应速率υ(C)=。
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: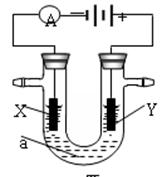
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为。
在X极附近观察到的实验现象是。
②Y电极上的电极反应式为。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是,电极反应式为。
②Y电极的材料是,电极反应式为。(说明:杂质发生的电极反应不必写出)
电解一段时间后,CuSO4溶液的浓度将(填“变大”、“变小”或“不变”)