天宫一号搭载的长征二号火箭使用的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R + 2N2O4= 3N2 + 4H2O + 2CO2,下列叙述错误的是
| A.此反应可在瞬间产生大量高温气体,推动火箭飞行 |
| B.此反应是氧化还原反应,N2O4做还原剂 |
| C.此反应是氧化还原反应,偏二甲肼做还原剂 |
| D.此反应中R的分子式为C2H8N2 |
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘处少。下列说法正确的是( )‘
| A.液滴中的Cl- 由a区向b区迁移 |
| B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-=4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-=Cu2+ |
据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染。其电池反应为:2Zn+O2=2ZnO,原料为锌粒、电解液和空气。则下列叙述正确的是(双选)( )
| A.锌为正极,空气进入负极反应 |
| B.负极反应为Zn-2e-=n2+ |
| C.正极发生氧化反应 |
| D.电解液肯定不是强酸 |
锌锰干电池在放电时,电池总反应方程式可以表示为Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是( )
| A.MnO2和NH4+ | B.Zn2+和NH4+ |
| C.Zn | D.碳棒 |
下图中,铁腐蚀由快到慢的顺序为(未标明的电解质溶液为水)( )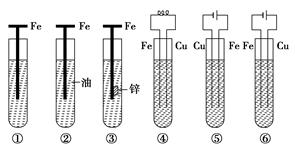
| A.⑥>④>①>②>③>⑤ |
| B.⑤>③>①>②>④>⑥ |
| C.⑤>④>①>②>③>⑥ |
| D.⑤>④>②>①>③>⑥ |
用普通食盐进行电解饱和食盐水的实验,食盐水装在U形管内,结果很快在某一电极附近出现食盐水浑浊现象。造成浑浊的难溶物主要是( )
| A.碳酸镁 | B.硫酸钡 |
| C.氢氧化镁 | D.碳酸钡 |