用含有A12O3、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
H2SO4溶解A12O3的离子方程式是
将KMnO4 氧化Fe2+的离子方程式补充完整:
 MnO4-+□Fe2++□ =
MnO4-+□Fe2++□ = Mn2++□Fe3+ +□
Mn2++□Fe3+ +□
上式中氧化剂是 ,氧化产物是 。
(3)已知:生成氢氧化物沉淀的pH
| |
Al(OH)3 |
Fe(OH)2 |
Fe(OH)3 |
| 开始沉淀时 |
3.4 |
6.3 |
1.5 |
| 完全沉淀时 |
4.7 |
8.3 |
2.8 |
注:金属离子的起始浓度为0.1mol·L-1
根据表中数据解释步骤Ⅱ的目的: 。
己知:一定条件下,MnO4 - 可与Mn2+反应生成MnO2。
① 向 Ⅲ 的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是 。
②Ⅳ 中加入MnSO4的目的是 。
常温下,取0.2mol·L-1HCl溶液与0.2mol·L-1MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
(1)混合溶液中由水电离出的c(H+)0.2mol·L-1HCl溶液中由水电离出的c(H+)(填“大于”、“小于”或“等于”)。
(2)求出混合物中下列算式的精确计算结果:
c(H+)−c(MOH)=,c(Cl-)−c(M+)=。
(3)若常温下取0.2mol·L-1MOH溶液与0.1mol·L-1HCl溶液等体积混合,测得混合溶液的pH<7,说明MOH的电离程度(填“大于”、“小于”或“等于”) MCl的水解程度。混合后的溶液中各离子浓度由大到小的顺序为。
进入2013年以来,我国中东部地区多次遭遇大范围、长时间的雾霾天气。车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。
(1)活性炭可处理大气污染物NO。在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
①结合上表数据,写出NO与活性炭反应的化学方程式。
②计算上述反应T2℃时的平衡常数K2=。
③根据上述信息判断,温度T1和T2的关系是(填序号)。
a.无法比较b.T1>T2c.T1<T2
(2)车辆排放的NO和CO在催化剂作用下可发生反应生成N2和CO2。在一体积为1L的密闭容积中,加入0.40mol的CO和0.40mol的NO,反应中N2的物质的量浓度的变化情况如图所示,
计算从反应开始到平衡时,平均反应速率v(NO)=。
(10分)A和甲是来自石油和煤的两种基本化工原料,A是气态烃,甲是液态烃。B和D是生活中两种常见的有机物,F是高分子化合物。相互转化关系如图所示(已知:R—CHO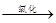 R—COOH)。
R—COOH)。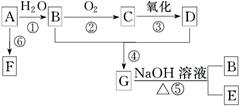
(1)A分子的电子式是____________。
(2)在反应①~⑥中,属于加成反应的是(填序号)。
(3)写出下列反应的化学方程式(有机物写结构简式)
②B→C:_______________________________________________________________;
④B+D→G:____________________________________________________________;
⑥A→F:________________________________________________________________。
镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。主要步骤如下: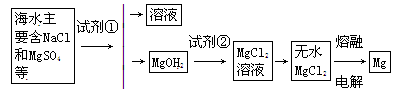
(1)为了使MgCl2转化为Mg(OH)2,试剂①可以选用。试剂②可以选用。
(2)验证MgCl2已完全转化为Mg(OH)2的方法是。
(3)由MgCl2溶液得到无水MgCl2的方法是。
食品添加剂必须严格按照食品安全国家标准(GB2760-2011)的规定使用。常作为食品添加剂中的防腐剂W,可以经过如下反应路线合成(部分反应条件略)。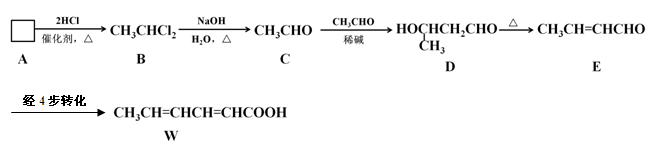
(1)已知A→B为加成反应,则A的结构简式为。
请用化学方程式表示实验室制取A的原理:。
(2)用D的同分异构体D1制备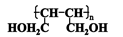 。
。
a、D1的结构简式为;
b、为避免副反应R-OH + R-OH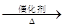 R-O-R + H2O的发生,合理的制备途径可以按照酯化反应、
R-O-R + H2O的发生,合理的制备途径可以按照酯化反应、
、的顺序依次进行(填反应类型)。
(3)已知乙烯不能被弱氧化剂氧化。依C→D→E的原理,由E制备W的4步转化为:
第1步:(用化学方程式表示);
第2步:消去反应;
第3步:(用化学方程式表示);
第4步:加适量稀酸酸化,提纯。